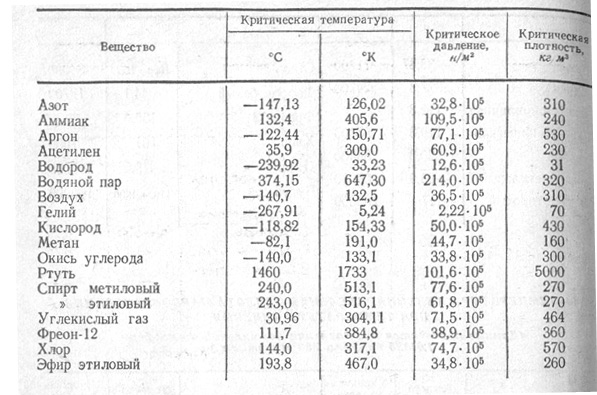
Температура кипения изобутана: Температура кипения изобутана – подробный ответ здесь!
Газоанализатор бутан
ГлавнаяСправочная информацияБутан
Газообразный углеводород бутан (C4H10) – представитель алканов, с характерным запахом, без цвета и вкуса входит в состав природного и нефтяного попутного газа. Его выделяют в процессе разделения на фракции нефтепродуктов, а в условиях лаборатории получают посредством ряда типичных химических реакций. По строению молекулы различают два изомера – н-бутан и изобутан, в практической химии название применяется в основном для н-бутана. Газовоздушная смесь с C4H10 взрывоопасна, для безопасного использования в производственных помещениях необходим газоанализатор бутана.
Свойства и характерные реакции
В нормальных условиях при 20°C, оба изомера находятся в газообразном состоянии, температура кипения у них разная, для н-бутана ее значение 0,5°C, а для изобутана – 11,7°C. Температура плавления также отличается и составляет -138,4°C и -159,6°C соответственно.
Вещество довольно инертно, в стандартных условиях не проявляет активности при контактах с концентрированными кислотами и щелочами, со щелочными расплавами и щелочными металлами. Не вступает в реакцию с галогенами, за исключением фтора и целым рядом других активных соединений. Химические свойства в полной мере соответствуют группе алканов, которой он принадлежит.
Среди характерных для алканов реакций – дегидрирование в присутствии катализатора, галогенирование, нитрование и сульфоокисление при повышенной температуре и, конечно же, горение. При горении выделяется углекислый газ и вода, если кислорода не хватает, то вместо углекислого газа CO 2 образуется угарный газ CO и углерод в виде сажи.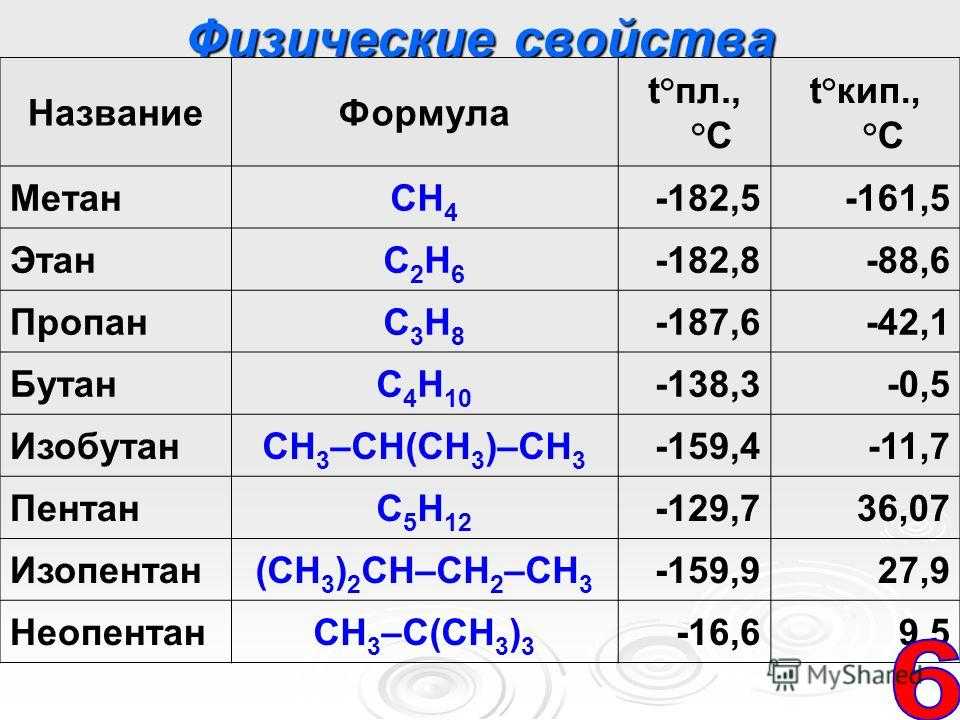
Применение
Востребован газ в качестве топлива, его смесь с пропаном используется для двигателей внутреннего сгорания, отопления и приготовления пищи в быту. С учетом того, что вещество относится к 4 классу опасности, его применяют в пищевой индустрии в качестве пищевых добавок – E943a(н-бутан) и E943b(изобутан).
Большое значение соединение имеет для производства безопасных холодильных установок, изобутан в чистом виде или в смеси с пропаном используются в качестве хладагента в теплообменниках холодильников и кондиционеров. Углеводород не представляет опасности для озонового слоя и постепенно вытесняет традиционные фреоны и аммиак. Широта применения требует, из-за его взрывоопасности, постоянного контроля концентрации. Газосигнализатор бутана, установленный в рабочем помещении, решает проблему безопасности.
Разработчик и производитель оборудования для газового анализа ИНКРАМ предлагает несколько технических решений для определения довзрывной концентрации НКПР в месте проведения работ. Среди предлагаемых решений можно выделить акусторезонансные датчики АРП,
Среди предлагаемых решений можно выделить акусторезонансные датчики АРП,
приборы серий В300 и С300,
моноканальные и многоканальные системы постоянного контроля СКВА.
Основные характеристики компонентов (фракций) сжиженных углеводородных газов
| Показатель | Этан | Этилен | Пропан | Пропилен | н-Бутан | Изобутан | н-Бутилен | Изобутилен | н-Пентан |
|---|---|---|---|---|---|---|---|---|---|
| Химическая формула | С2Н6 | С2Н4 | С3Н8 | С3Н6 | С4Н10 | С4Н10 | С4Н8 | С4Н8 | С5Н12 |
| Молекулярная масса M | 30,068 | 28,054 | 44,097 | 42,081 | 58,124 | 58,124 | 56,108 | 56,104 | 72,146 |
| Молярный объем VМ, м³/кмоль | 22,174 | 22,263 | 21,974 | 21,50 | 21,743 | 22,442 | 22,442 | 20,87 | |
| Плотность газовой фазы, кг/м³: | |||||||||
| при 0 °С и 101,3 кПа рu0 | 1,356 | 1,260 | 2,0037 | 1,9149 | 2,7023 | 2,685 | 2,55 | 2,5022 | 3,457 |
| при 20 °С и 101,3 кПа pu20 | 1,263 | 1,174 | 1,872 | 1,784 | 2,519 | 2,486 | 2,329 | 2,329 | 3,221 |
| Плотность жидкой фазы, кг/м³, при 0 °С и 101,3 кПа, рж | 0,546 | 0,566 | 0,528 | 0,609 | 0,601 | 0,582 | 0,646 | 0,646 | 0,6455 |
| Относительная плотность dn | 1,0487 | 0,9753 | 1,5545 | 1,4811 | 2,0995 | 2,0634 | 1,9336 | 1,9336 | 2,6736 |
| Удельная газовая постоянная R, Дж/(кг×К) | 271,18 | 261,26 | 184,92 | 193,77 | 140,3 | 140,3 | 145,33 | 145,33 | 113,014 |
| Температура, °С, при 101,3 кПа: | |||||||||
| кипения tкип | –88,6 | –104 | –42,1 | –47,7 | –0,5 | –11,73 | –6,9 | –3,72 | –36,07 |
| плавления tпл | –183,3 | –169 | –187,7 | –185,3 | –138,3 | –193,6 | –140,4 | –129,7 | |
| Температура критическая tкр, °С | +32,3 | +9,9 | +96,84 | +91,94 | +152,01 | +134,98 | +144,4 | +155,0 | +196,6 |
| Давление критическое ркр, МПа | 4,82 | 5,033 | 4,21 | 4,54 | 3,747 | 3,60 | 3,945 | 4,10 | 3,331 |
| Теплота плавления Qпл, кДж/кг | 122,6 | 119,7 | 10,64 | — | — | — | — | — | — |
| Теплота сгорания, МДж/м³: | |||||||||
| высшая Qвр | 69,69 | 63,04 | 99,17 | 91,95 | 128,5 | 128,28 | 121,4 | 121,4 | 130,0 |
| низшая Qнр | 63,65 | 59,53 | 91,14 | 86,49 | 118,53 | 118,23 | 113,83 | 113,83 | 146,18 |
| Теплота сгорания, МДж/кг: | |||||||||
| высшая Qвр | 51,92 | 51,24 | 50,37 | 49,95 | 49,57 | 49,45 | 49,31 | 49,31 | 49,20 |
| низшая Qнр | 47,42 | 47,23 | 46,3 | 46,04 | 45,76 | 45,68 | 45,45 | 45,45 | 45,38 |
| Число Воббе, МДж/м³: | |||||||||
| высшее W0в | 68,12 | 64,03 | 79,8 | 75,72 | 89,18 | 93,53 | 87,64 | 87,64 | 93,73 |
| низшее W0н | 62,45 | 60,03 | 73,41 | 70,92 | 82,41 | 86,43 | 81,94 | 81,94 | 86,56 |
| Удельная теплоемкость газа cГ, кДж/(кг°С), при 0 °С и: | |||||||||
| постоянном давлении ср | 1,6506 | 1,4658 | 1,554 | 1,4322 | 1,596 | 1,5690 | 1,4868 | 1,6044 | 1,6002 |
| постоянном объеме сv | 1,3734 | 1,1634 | 1,365 | 1,222 | 1,4574 | 1,4574 | 1,3398 | 1,445 | 1,424 |
| То же, жидкой фазы сж, кДж/(кг °С), при 0 °С и 101,3 кПа | 3,01 | 2,415 | 2,23 | — | 2,239 | 2,239 | — | — | 2,668 |
| Показатель адиабаты, К, при 0 °С и 101,3 кПа | 1,202 | 1,26 | 1,138 | 1,172 | 1,095 | 1,095 | 1,11 | 1,11 | 1,124 |
Теоретически необходимое количество воздуха для горения Lт. в., м³/м³ в., м³/м³ |
16,66 | 14,28 | 23,8 | 22,42 | 30,94 | 30,94 | 28,46 | 28,56 | 38,08 |
| То же, кислорода |
3,5 | 3,0 | 5,0 | 4,5 | 6,5 | 6,5 | 6,0 | 6,0 | 8,0 |
| Объем влажных продуктов сгорания, м³/м³, при а = 1: | |||||||||
| CO2 | 2,0 | 2,0 | 3,0 | 3,0 | 4,0 | 4,0 | 4,0 | 4,0 | 5,0 |
| H2O | 3,0 | 2,0 | 4,0 | 3,0 | 5,0 | 5,0 | 4,0 | 4,0 | 6,0 |
| N2 | 13,16 | 11,28 | 18,8 | 16,92 | 24,44 | 24,44 | 20,68 | 20,68 | 30,08 |
| Всего | 18,16 | 15,28 | 25,80 | 22,92 | 33,44 | 33,44 | 28,68 | 28,68 | 41,08 |
| Скрытая теплота испарения при 101,3 кПа: | |||||||||
| кДж/кг | 487,2 | 483,0 | 428,4 | 441,0 | 390,6 | 383,2 | 411,6 | 299,0 | 361,2 |
| кДж/л | 230,2 | 221,8 | 220,1 | 241,1 | 229,7 | 215,0 | 255,4 | 239,4 | — |
| Объем паров с 1 кг сжиженных газов при нормальных условиях Vп, м³ | 0,745 | 0,8 | 0,51 | 0,52 | 0,386 | 0,386 | 0,4 | 0,4 | 0,312 |
| То же, с 1 л | 0,31 | 0,34 | 0,269 | 0,287 | 0,235 | 0,229 | 0,254 | 0,254 | 0,198 |
Изобутан — Википедия
Basculer la table des matières Статья из Википедии, свободная энциклопедия.
L’ isobutane ou 2-méthylpropane est un hydrocarbure de formule brute C 4 H 10 que l’on trouve sous forme de gaz dans привычка к температуре и давлению. Это изомера бутана. В нем используется жидкий хладагент под названием R600a (или технология «Greenfreeze»).
Изобутан является реагентом основания для производства пероксида ди- трет--бутила (не входит в состав важных карбюраторов или играет роль антидетонанта), изобутена (катализатор дегидрогенизации) et de l’acide méthacrylique (пароксидирование [15] ).
C’est aussi unfrigorigene Fluide et un aerosol Ussi un frigorigene et un aerosol utilise en aux CFC et aux HFC to ограничитель воздействия на озоновый слой и l’effet de Serre notamment à call de son faible impact sur l’environnement:
- ODP или способность разрушать озоновый слой: 0 (R600a);
- GWP или PRG (глобальный потенциал восстановления): 3 (R600a).

Сотрудничество между предприятиями Foron и ONG Greenpeace, разрешение на создание в 1993 году технологии Greenfreeze, использующей хладагент.
Является источником радикала трет -бутил (CH 3 ) 3 C- имеет большое значение в органическом синтезе для выполнения роли группового протектора грации и волосяного покрова.
Давление насыщения паров [16] :
| Температура | Прессион | Температура | Прессион |
|---|---|---|---|
| −113,15 °С | 0,1 кПа | −38,15 °С | 31,1 кПа |
| −108,15 °С | 0,1 кПа | −33,15 °С | 39,8 кПа |
| −103,15 °С | 0,3 кПа | −28,15 °С | 50,3 кПа |
| −98,15 °С | 0,4 кПа | −23,15 °С | 62,9 кПа |
| −93,15 °С | 0,7 кПа | −18,15 °С | 77,8 кПа |
| −88,15 °С | 1,1 кПа | −13,15 °С | 95,4 кПа |
| −83,15 °С | 1,7 кПа | −8,15 °С | 116 кПа |
| −78,15 °С | 2,5 кПа | −3,15 °С | 140 кПа |
| −73,15 °С | 3,7 кПа | 1,85 °С | 167 кПа |
| −68,15 °С | 5,3 кПа | 6,85 °С | 198 кПа |
| −63,15 °С | 7,4 кПа | 11,85 °С | 234 кПа |
| −58,15 °С | 10,2 кПа | 16,85 °С | 274 кПа |
| −53,15 °С | 13,8 кПа | 21,85 °С | 319 кПа |
| −48,15 °С | 18,3 кПа | 26,85 °С | 370 кПа |
| −43,15 °С | 24,0 кПа | 50 °С | 678 кПа [4] |
Изобутан получен двумя способами [15] :
- по номиналу дистилляция нефтяной фракции аппеляционного газа сжиженной нефти;
- каталитическая изомеризация бутановой кислоты.

Характер легковоспламеняющихся веществ требует особого внимания к рискам и соответствующих методов вмешательства: pas de flamme, pas de chalumeau, запрет дыма в мастерской вмешательства, qui doit être ventilé et équipé de dispositifs d’extraction Basse.
Pour toute Intervention sur une unité hermétique, on préfèrera l’emploi de sans brasures, mais ces dernières restent возможных sous условий [17] .
- ↑ а и б ИЗОБУТАН, Fiches internationales de sécurité chimique.
- ↑ (en) David R. Lide, Handbook of Chemistry and Physics , Boca Raton, CRC, , 89 e ed. , 2736 стр. (ISBN 978-1-4200-6679-1) , стр. 9-50.
- ↑ Masse molaire calculée d’après « Атомные веса элементов 2007 » , на сайте www.
 chem.qmul.ac.uk.
chem.qmul.ac.uk. - ↑ а б в г д е ж г е ч Entrée «Isobutane» dans la base de données de produits chimiques GESTIS de la IFA (allemand responsable de la sécurité et de la santé au travail) (английский, английский), accès le 17 avril 2009 (18) Script (JavaScript) .
- ↑ a b et c « Изобутан », банк данных по опасным веществам (консультируйтесь по телефону ) .
- ↑ a b et c (en) Роберт Х. Перри и Дональд В. Грин, Справочник инженеров-химиков Perry , États-Unis, McGraw-Hill, , 7 e ed. , 2400 р. (ISBN 0-07-049841-5) , стр. 2-50.
- ↑ (en) Ивона Овчарек и Кристина Блажей, « Рекомендуемые критические давления.
 Часть I. Алифатические углеводороды », J. Phys. хим. Ссылка Данные , том. 35, н o 4, , с. 1461 (DOI 10.1063/1.2201061) .
Часть I. Алифатические углеводороды », J. Phys. хим. Ссылка Данные , том. 35, н o 4, , с. 1461 (DOI 10.1063/1.2201061) . - ↑ (en) Ивона Овчарек и Кристина Блажей, « Рекомендуемые критические температуры. Часть I. Алифатические углеводороды », J. Phys. хим. Ссылка Данные , том. 32, n o 4, , с. 1411 (DOI 10.1063/1.1556431) .
- ↑ a b c d e et f « Изобутан », surnist.gov (консультируйтесь по адресу ) .

- ↑ (en) Carl L. Yaws, Справочник по термодинамическим диаграммам: неорганические соединения и элементы , vol. 1, Хьюстон, Техас, Gulf Pub. Ко., , 384 с. (ISBN 0-88415-857-8) .
- ↑ «изобутан», sur ESIS (консультация от 15 февраля 2009 г.).
- ↑ Нумерационный индекс 601-004-00-0 в таблице 3.1 приложения VI к регламенту CE n o 1272/2008 (16 декабря 2008 г.)
- ↑ Нумерационный индекс 601-004-01-8 в таблице 3.1 приложения VI к регламенту CE n или 1272/2008 (16 декабря 2008 г.).
- ↑ «Изобутан» в базе данных химических продуктов Reptox de la CSST (Квебекский орган, ответственный за безопасность и безопасность труда), Consulté le 23 avril 2009.
- ↑ a et b Карл Грисбаум, Арно Бер, Дитер Биденкапп, Хайнц-Вернер Фогес, Доротея Гарбе, Кристиан Паец, Герд Коллин, Дитер Майер и Хартмут Хёке, Энциклопедия промышленной химии Ульмана , Углеводороды, Wiley-VCH Verlag, .

- ↑ (en) Дэвид Р. Лайд, CRC Handbook of Chemistry and Physics , CRC Press, , 90 e ed. , 2804 с. , Relié (ISBN 978-1-4200-9084-0) , стр. 6-109.
- ↑ « Lesfluides frigorigènes hydrocarbures », sur abcclim.net (проконсультируйтесь с ) .
- Бутан
Алканы простые разветвления Метиловая группа в позиции 2 | ||
|---|---|---|
| ||
Алканы простые разветвления Группа метильных атомов углерода | ||
|---|---|---|
| ||
- Portail de la chimie
ИЗОБУТАН | 75-28-5
Химические свойства
бесцветный газ без запаха (или бесцветная криогенная жидкость)
Химические свойства
2-Метилпропан (изобутан), C4h20, легковоспламеняющийся газ,
встречается в небольших количествах в природном газе и сырой нефти.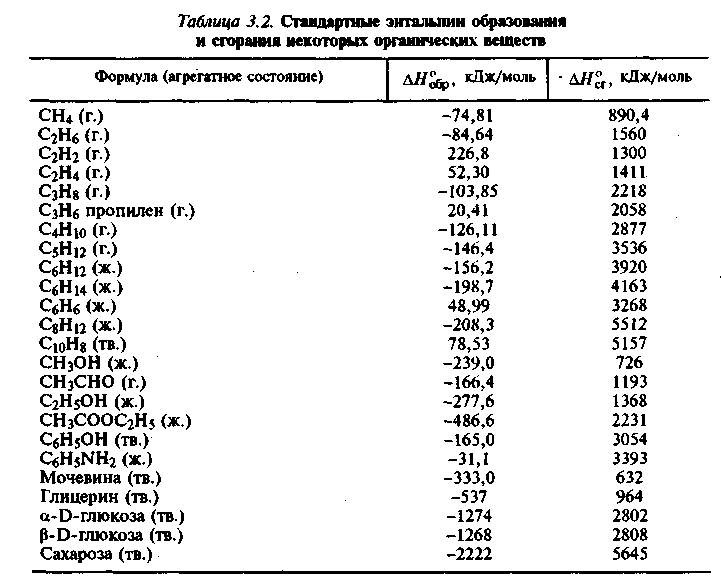 Это
был обнаружен в городской атмосфере при концентрациях
44–74 частей на миллиард. Он также развивается из природных источников и
было измерено в выхлопных газах дизельных двигателей на уровне 1,4–11 частей на миллион.
и в сигаретном дыме при 10 ppm. Раздел
коэффициент пропана между оливковым маслом и воздухом при 37 ℃ составляет
12 с использованием метода, описанного Сато и Накадзимой, и
Perbellini et al. Нижний предел взрываемости
18 000 частей на миллион в воздухе.
Это
был обнаружен в городской атмосфере при концентрациях
44–74 частей на миллиард. Он также развивается из природных источников и
было измерено в выхлопных газах дизельных двигателей на уровне 1,4–11 частей на миллион.
и в сигаретном дыме при 10 ppm. Раздел
коэффициент пропана между оливковым маслом и воздухом при 37 ℃ составляет
12 с использованием метода, описанного Сато и Накадзимой, и
Perbellini et al. Нижний предел взрываемости
18 000 частей на миллион в воздухе.
Использование
Изобутан встречается в нефти, природном газе и продуктах крекинга нефти. Он используется в качестве топливного газа или сжиженного нефтяного газа. Он также используется в органическом синтезе.
Использование
В производстве пропиленгликолей и оксиды и пенополиуретаны и смолы; как компонент моторных топлив и аэрозольных пропеллентов; в качестве промышленного газовоза и общего источник топлива
Использование
Органический синтез, хладагенты, моторные топлива,
аэрозольный пропеллент, синтетический каучук, жидкость для калибровки приборов.
Определение
ChEBI: Алкан, который представляет собой пропан, замещенный метильной группой в положении 2.
Общее описание
ИЗОБУТАН представляет собой бесцветный газ со слабым нефтяным запахом. ИЗОБУТАН поставляется в виде сжиженного газа под давлением паров. Контакт с жидкостью может вызвать обморожение. ИЗОБУТАН легко воспламеняется. Пары тяжелее воздуха. Любая утечка может быть как жидкостью, так и паром. ИЗОБУТАН может вызвать удушье при вытеснении воздуха. При длительном воздействии огня или сильного нагрева контейнеры могут сильно разорваться и взорваться.
Реакции воздуха и воды
Легко воспламеняется.
Профиль реактивности
ИЗОБУТАН несовместим со следующими веществами: Сильные окислители (например, нитраты и перхлораты), хлор, фтор (карбонил никеля + кислород).
Опасность
Легковоспламеняющиеся, пожароопасные и взрывоопасность; пределы взрываемости в воздухе 1,9–8,5%.
Опасность для здоровья
Угнетение центральной нервной системы в диапазоне от головокружения и нарушения координации до анестезии и остановки дыхания, в зависимости от концентрации и степени вдыхания. Нерегулярное сердцебиение встречается редко, но является опасным осложнением при уровне анестезии.
Опасность для здоровья
Изобутан, как и другие насыщенные алифатические алканы, нетоксичен. Это асфиксия. Воздействие высоких концентраций 1% в воздухе может вызвать наркоз и сонливость. Кроме этого, нет сообщений о каких-либо неблагоприятных последствиях для здоровья от воздействия этого газа.
Опасность пожара
ЧРЕЗВЫЧАЙНО ОГНЕОПАСНО.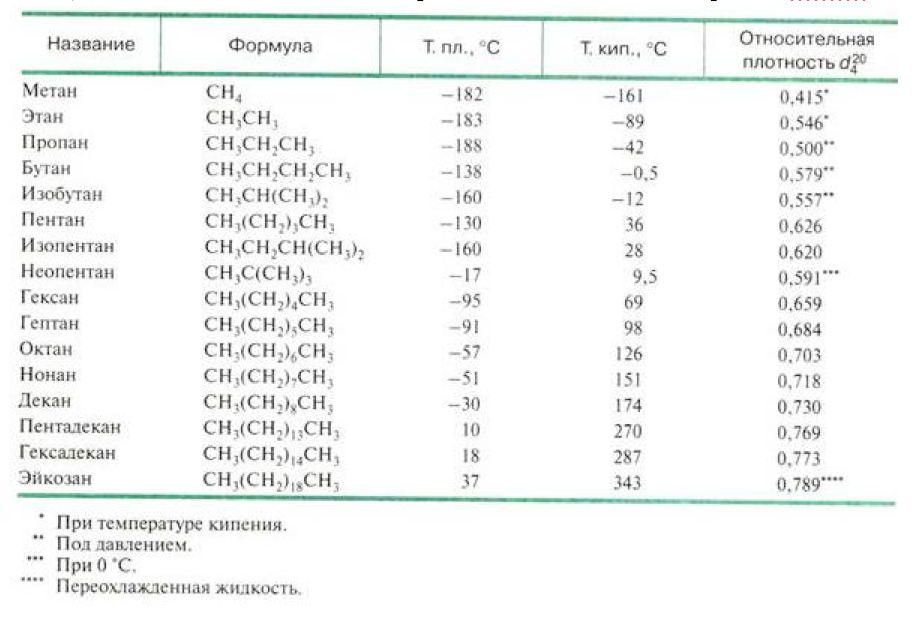 Легко воспламеняется от тепла, искр или пламени. Образует взрывоопасные смеси с воздухом. Пары сжиженного газа изначально тяжелее воздуха и распространяются по земле. ВНИМАНИЕ! Водород (UN1049), дейтерий (UN1957), водород, охлажденная жидкость (UN1966) и метан (UN1971) легче воздуха и будут подниматься вверх. Водородные и дейтериевые пожары трудно обнаружить, поскольку они горят невидимым пламенем. Используйте альтернативный метод обнаружения (тепловизионная камера, ручка метлы и т. д.). Пары могут попасть к источнику воспламенения и вспыхнуть обратно. Баллоны, подвергшиеся воздействию огня, могут выпускать горючие газы через устройства сброса давления. Контейнеры могут взорваться при нагревании. Разорванные цилиндры могут взлететь.
Легко воспламеняется от тепла, искр или пламени. Образует взрывоопасные смеси с воздухом. Пары сжиженного газа изначально тяжелее воздуха и распространяются по земле. ВНИМАНИЕ! Водород (UN1049), дейтерий (UN1957), водород, охлажденная жидкость (UN1966) и метан (UN1971) легче воздуха и будут подниматься вверх. Водородные и дейтериевые пожары трудно обнаружить, поскольку они горят невидимым пламенем. Используйте альтернативный метод обнаружения (тепловизионная камера, ручка метлы и т. д.). Пары могут попасть к источнику воспламенения и вспыхнуть обратно. Баллоны, подвергшиеся воздействию огня, могут выпускать горючие газы через устройства сброса давления. Контейнеры могут взорваться при нагревании. Разорванные цилиндры могут взлететь.
Профиль безопасности
Удушающий. А
обычный загрязнитель воздуха. очень опасный
опасность пожара и взрыва при воздействии
тепла, пламени или окислителей. Чтобы бороться с огнем, остановитесь
расход газа. При нагревании до разложения
он выделяет едкий дым и раздражающие пары.
При нагревании до разложения
он выделяет едкий дым и раздражающие пары.
Источник
Калифорнийский реформулированный бензин фазы II содержал 2-метилпропан в концентрации 1,04 г/кг. Интенсивность выбросов выхлопных газов в газовой фазе автомобилей с бензиновым двигателем, оснащенных катализатора – 130 мкг/км (Schauer et al., 2002).
Экологическая судьба
Фотолитический. На основе константы скорости фотоокисления 2,34 x 10 -12 см 3 /молекула?сек с OH
радикалов в летнее дневное время время жизни в атмосфере составляет 59 ч (Альтшуллер, 1991). При атмосферном
давление и 300 K, Darnall et al. (1978) сообщили о константе скорости 2,52 x 10 -12 см 3 /молекула?сек.
для той же реакции. Константы скорости 1,28 x 10 -9 и 6,03 x 10 -12 л/молекула?сек.
для реакции 2-метилпропана с радикалами ОН на воздухе при 300 и 296 К соответственно
(Грейнер, 1967, 1970). Константы скорости 7,38 x 10 -13 и 6,50 x 10 -17 см 3 /молекула?сек были
сообщалось о реакции 2-метилпропана с OH и NO3 соответственно (Sablji? and Güsten,
1990).
Константы скорости 7,38 x 10 -13 и 6,50 x 10 -17 см 3 /молекула?сек были
сообщалось о реакции 2-метилпропана с OH и NO3 соответственно (Sablji? and Güsten,
1990).
Химический/физический. При полном сгорании на воздухе образуются углекислый газ и водяной пар. 2-
Метилпропан не гидролизуется, поскольку не содержит гидролизуемой функциональной группы.
Растворимость в органических веществах
(мольная доля):
В 1-бутаноле: 0,0897, 0,0491 и 0,0308 при 25, 30 и 70°С соответственно; хлорбензол: 0,157,
0,0837 и 0,0542 при 25, 30 и 70 °С соответственно; и октановое число: 0,301, 0,161 и 0,101 при 25,
30 и 70 °С соответственно (Хайдук и др., 1988).
В 1-бутаноле: 0,0889 и 0,0486 при 25 и 70 °C соответственно; в хлорбензоле: 0,162 и 0,0853
при 25 и 70 °С соответственно; а в четыреххлористом углероде: 0,238 и 0,132 при 25 и 70 °С,
соответственно (Бле и Хайдук, 1983).


 chem.qmul.ac.uk.
chem.qmul.ac.uk. Часть I. Алифатические углеводороды », J. Phys. хим. Ссылка Данные , том. 35, н o 4, , с. 1461 (DOI 10.1063/1.2201061) .
Часть I. Алифатические углеводороды », J. Phys. хим. Ссылка Данные , том. 35, н o 4, , с. 1461 (DOI 10.1063/1.2201061) .