Пропан плюс кислород: Горение пропана в кислороде
Пропан, структурная формула, химические, физические свойства
1
H
ВодородВодород
1,008
1s1
2,2
Бесцветный газ
t°пл=-259°C
t°кип=-253°C
2
He
ГелийГелий
4,0026
1s2
Бесцветный газ
t°кип=-269°C
3
Li
ЛитийЛитий
6,941
2s1
0,99
Мягкий серебристо-белый металл
t°пл=180°C
t°кип=1317°C
4
Be
БериллийБериллий
9,0122
2s2
1,57
Светло-серый металл
t°пл=1278°C
t°кип=2970°C
5
B
БорБор
10,811
2s2 2p1
2,04
Темно-коричневое аморфное вещество
t°пл=2300°C
t°кип=2550°C
6
C
УглеродУглерод
12,011
2s2 2p2
2,55
Прозрачный (алмаз) / черный (графит) минерал
t°пл=3550°C
7
N
АзотАзот
14,007
2s2 2p3
3,04
Бесцветный газ
t°пл=-210°C
t°кип=-196°C
8
O
КислородКислород
15,999
2s2 2p4
3,44
Бесцветный газ
t°пл=-218°C
t°кип=-183°C
9
F
ФторФтор
18,998
2s2 2p5
4,0
Бледно-желтый газ
t°пл=-220°C
t°кип=-188°C
10
Ne
НеонНеон
20,180
2s2 2p6
Бесцветный газ
t°пл=-249°C
t°кип=-246°C
11
Na
НатрийНатрий
22,990
3s1
0,93
Мягкий серебристо-белый металл
t°пл=98°C
t°кип=892°C
12
Mg
МагнийМагний
24,305
3s2
1,31
Серебристо-белый металл
t°пл=649°C
t°кип=1107°C
13
Al
АлюминийАлюминий
26,982
3s2 3p1
1,61
Серебристо-белый металл
t°пл=660°C
t°кип=2467°C
14
Si
КремнийКремний
28,086
3s2 3p2
1,9
Коричневый порошок / минерал
t°пл=1410°C
t°кип=2355°C
15
P
ФосфорФосфор
30,974
3s2 3p3
2,2
Белый минерал / красный порошок
t°пл=44°C
t°кип=280°C
16
S
СераСера
32,065
3s2 3p4
2,58
Светло-желтый порошок
t°пл=113°C
t°кип=445°C
17
Cl
ХлорХлор
35,453
3s2 3p5
3,16
Желтовато-зеленый газ
t°пл=-101°C
t°кип=-35°C
18
Ar
АргонАргон
39,948
3s2 3p6
Бесцветный газ
t°пл=-189°C
t°кип=-186°C
19
K
КалийКалий
39,098
4s1
0,82
Мягкий серебристо-белый металл
t°пл=64°C
t°кип=774°C
20
Ca
КальцийКальций
40,078
4s2
1,0
Серебристо-белый металл
t°пл=839°C
t°кип=1487°C
21
Sc
СкандийСкандий
44,956
3d1 4s2
1,36
Серебристый металл с желтым отливом
t°пл=1539°C
t°кип=2832°C
22
Ti
ТитанТитан
47,867
3d2 4s2
1,54
Серебристо-белый металл
t°пл=1660°C
t°кип=3260°C
23
V
ВанадийВанадий
50,942
3d3 4s2
1,63
Серебристо-белый металл
t°пл=1890°C
t°кип=3380°C
24
Cr
ХромХром
51,996
3d5 4s1
1,66
Голубовато-белый металл
t°пл=1857°C
t°кип=2482°C
25
Mn
МарганецМарганец
54,938
3d5 4s2
1,55
Хрупкий серебристо-белый металл
t°пл=1244°C
t°кип=2097°C
26
Fe
ЖелезоЖелезо
55,845
3d6 4s2
1,83
Серебристо-белый металл
t°пл=1535°C
t°кип=2750°C
27
Co
КобальтКобальт
58,933
3d7 4s2
1,88
Серебристо-белый металл
t°пл=1495°C
t°кип=2870°C
28
Ni
НикельНикель
58,693
3d8 4s2
1,91
Серебристо-белый металл
t°пл=1453°C
t°кип=2732°C
29
Cu
МедьМедь
63,546
3d10 4s1
1,9
Золотисто-розовый металл
t°пл=1084°C
t°кип=2595°C
30
Zn
ЦинкЦинк
65,409
3d10 4s2
1,65
Голубовато-белый металл
t°пл=420°C
t°кип=907°C
31
Ga
ГаллийГаллий
69,723
4s2 4p1
1,81
Белый металл с голубоватым оттенком
t°пл=30°C
t°кип=2403°C
32
Ge
ГерманийГерманий
72,64
4s2 4p2
2,0
Светло-серый полуметалл
t°пл=937°C
t°кип=2830°C
33
As
МышьякМышьяк
74,922
4s2 4p3
2,18
Зеленоватый полуметалл
t°субл=613°C
(сублимация)
34
Se
СеленСелен
78,96
4s2 4p4
2,55
Хрупкий черный минерал
t°пл=217°C
t°кип=685°C
35
Br
БромБром
79,904
4s2 4p5
2,96
Красно-бурая едкая жидкость
t°пл=-7°C
t°кип=59°C
36
Kr
КриптонКриптон
83,798
4s2 4p6
3,0
Бесцветный газ
t°пл=-157°C
t°кип=-152°C
37
Rb
РубидийРубидий
85,468
5s1
0,82
Серебристо-белый металл
t°пл=39°C
t°кип=688°C
38
Sr
СтронцийСтронций
87,62
5s2
0,95
Серебристо-белый металл
t°пл=769°C
t°кип=1384°C
39
Y
ИттрийИттрий
88,906
4d1 5s2
1,22
Серебристо-белый металл
t°пл=1523°C
t°кип=3337°C
40
Zr
ЦирконийЦирконий
91,224
4d2 5s2
1,33
Серебристо-белый металл
t°пл=1852°C
t°кип=4377°C
41
Nb
НиобийНиобий
92,906
4d4 5s1
1,6
Блестящий серебристый металл
t°пл=2468°C
t°кип=4927°C
42
Mo
МолибденМолибден
95,94
4d5 5s1
2,16
Блестящий серебристый металл
t°пл=2617°C
t°кип=5560°C
43
Tc
ТехнецийТехнеций
98,906
4d6 5s1
1,9
Синтетический радиоактивный металл
t°пл=2172°C
t°кип=5030°C
44
Ru
РутенийРутений
101,07
4d7 5s1
2,2
Серебристо-белый металл
t°пл=2310°C
t°кип=3900°C
45
Rh
РодийРодий
102,91
4d8 5s1
2,28
Серебристо-белый металл
t°пл=1966°C
t°кип=3727°C
46
Pd
ПалладийПалладий
106,42
4d10
2,2
Мягкий серебристо-белый металл
t°пл=1552°C
t°кип=3140°C
47
Ag
СереброСеребро
107,87
4d10 5s1
1,93
Серебристо-белый металл
t°пл=962°C
t°кип=2212°C
48
Cd
КадмийКадмий
112,41
4d10 5s2
1,69
Серебристо-серый металл
t°пл=321°C
t°кип=765°C
49
In
ИндийИндий
114,82
5s2 5p1
1,78
Мягкий серебристо-белый металл
t°пл=156°C
t°кип=2080°C
50
Sn
ОловоОлово
118,71
5s2 5p2
1,96
Мягкий серебристо-белый металл
t°пл=232°C
t°кип=2270°C
51
Sb
СурьмаСурьма
121,76
5s2 5p3
2,05
Серебристо-белый полуметалл
t°пл=631°C
t°кип=1750°C
52
Te
ТеллурТеллур
127,60
5s2 5p4
2,1
Серебристый блестящий полуметалл
t°пл=450°C
t°кип=990°C
53
I
ИодИод
126,90
5s2 5p5
2,66
Черно-серые кристаллы
t°пл=114°C
t°кип=184°C
54
Xe
КсенонКсенон
131,29
5s2 5p6
2,6
Бесцветный газ
t°пл=-112°C
t°кип=-107°C
55
Cs
ЦезийЦезий
132,91
6s1
0,79
Мягкий серебристо-желтый металл
t°пл=28°C
t°кип=690°C
56
Ba
БарийБарий
137,33
6s2
0,89
Серебристо-белый металл
t°пл=725°C
t°кип=1640°C
57
La
ЛантанЛантан
138,91
5d1 6s2
1,1
Серебристый металл
t°пл=920°C
t°кип=3454°C
58
Ce
ЦерийЦерий
140,12
f-элемент
Серебристый металл
t°пл=798°C
t°кип=3257°C
59
Pr
ПразеодимПразеодим
140,91
f-элемент
Серебристый металл
t°пл=931°C
t°кип=3212°C
60
Nd
НеодимНеодим
144,24
f-элемент
Серебристый металл
t°пл=1010°C
t°кип=3127°C
61
Pm
ПрометийПрометий
146,92
f-элемент
Светло-серый радиоактивный металл
t°пл=1080°C
t°кип=2730°C
62
Sm
СамарийСамарий
150,36
Серебристый металл
t°пл=1072°C
t°кип=1778°C
63
Eu
ЕвропийЕвропий
151,96
f-элемент
Серебристый металл
t°пл=822°C
t°кип=1597°C
64
Gd
ГадолинийГадолиний
157,25
f-элемент
Серебристый металл
t°пл=1311°C
t°кип=3233°C
65
Tb
ТербийТербий
158,93
f-элемент
Серебристый металл
t°пл=1360°C
t°кип=3041°C
66
Dy
ДиспрозийДиспрозий
162,50
f-элемент
Серебристый металл
t°пл=1409°C
t°кип=2335°C
67
Ho
ГольмийГольмий
164,93
f-элемент
Серебристый металл
t°пл=1470°C
t°кип=2720°C
68
Er
ЭрбийЭрбий
167,26
f-элемент
Серебристый металл
t°пл=1522°C
t°кип=2510°C
69
Tm
ТулийТулий
168,93
f-элемент
Серебристый металл
t°пл=1545°C
t°кип=1727°C
70
Yb
ИттербийИттербий
173,04
f-элемент
Серебристый металл
t°пл=824°C
t°кип=1193°C
71
Lu
ЛютецийЛютеций
174,96
f-элемент
Серебристый металл
t°пл=1656°C
t°кип=3315°C
72
Hf
ГафнийГафний
178,49
5d2 6s2
Серебристый металл
t°пл=2150°C
t°кип=5400°C
73
Ta
ТанталТантал
180,95
5d3 6s2
Серый металл
t°пл=2996°C
t°кип=5425°C
74
W
ВольфрамВольфрам
183,84
5d4 6s2
2,36
Серый металл
t°пл=3407°C
t°кип=5927°C
75
Re
РенийРений
186,21
5d5 6s2
Серебристо-белый металл
t°пл=3180°C
t°кип=5873°C
76
Os
ОсмийОсмий
190,23
5d6 6s2
Серебристый металл с голубоватым оттенком
t°пл=3045°C
t°кип=5027°C
77
Ir
ИрридийИрридий
192,22
5d7 6s2
Серебристый металл
t°пл=2410°C
t°кип=4130°C
78
Pt
ПлатинаПлатина
195,08
5d9 6s1
2,28
Мягкий серебристо-белый металл
t°пл=1772°C
t°кип=3827°C
79
Au
ЗолотоЗолото
196,97
5d10 6s1
2,54
Мягкий блестящий желтый металл
t°пл=1064°C
t°кип=2940°C
80
Hg
РтутьРтуть
200,59
5d10 6s2
2,0
Жидкий серебристо-белый металл
t°пл=-39°C
t°кип=357°C
81
Tl
ТаллийТаллий
204,38
6s2 6p1
Серебристый металл
t°пл=304°C
t°кип=1457°C
82
Pb
СвинецСвинец
207,2
6s2 6p2
2,33
Серый металл с синеватым оттенком
t°пл=328°C
t°кип=1740°C
83
Bi
ВисмутВисмут
208,98
6s2 6p3
Блестящий серебристый металл
t°пл=271°C
t°кип=1560°C
84
Po
ПолонийПолоний
208,98
6s2 6p4
Мягкий серебристо-белый металл
t°пл=254°C
t°кип=962°C
85
At
АстатАстат
209,98
6s2 6p5
2,2
Нестабильный элемент, отсутствует в природе
t°пл=302°C
t°кип=337°C
86
Rn
РадонРадон
222,02
6s2 6p6
2,2
Радиоактивный газ
t°пл=-71°C
t°кип=-62°C
87
Fr
ФранцийФранций
223,02
7s1
0,7
Нестабильный элемент, отсутствует в природе
t°пл=27°C
t°кип=677°C
88
Ra
РадийРадий
226,03
7s2
0,9
Серебристо-белый радиоактивный металл
t°пл=700°C
t°кип=1140°C
89
Ac
АктинийАктиний
227,03
6d1 7s2
1,1
Серебристо-белый радиоактивный металл
t°пл=1047°C
t°кип=3197°C
90
Th
ТорийТорий
232,04
f-элемент
Серый мягкий металл
91
Pa
ПротактинийПротактиний
231,04
f-элемент
Серебристо-белый радиоактивный металл
92
U
УранУран
238,03
f-элемент
1,38
Серебристо-белый металл
t°пл=1132°C
t°кип=3818°C
93
Np
НептунийНептуний
237,05
f-элемент
Серебристо-белый радиоактивный металл
94
Pu
ПлутонийПлутоний
244,06
f-элемент
Серебристо-белый радиоактивный металл
95
Am
АмерицийАмериций
243,06
f-элемент
Серебристо-белый радиоактивный металл
96
Cm
КюрийКюрий
247,07
f-элемент
Серебристо-белый радиоактивный металл
97
Bk
БерклийБерклий
247,07
f-элемент
Серебристо-белый радиоактивный металл
98
Cf
КалифорнийКалифорний
251,08
f-элемент
Нестабильный элемент, отсутствует в природе
99
Es
ЭйнштейнийЭйнштейний
252,08
f-элемент
Нестабильный элемент, отсутствует в природе
100
Fm
ФермийФермий
257,10
f-элемент
Нестабильный элемент, отсутствует в природе
101
Md
МенделевийМенделевий
258,10
f-элемент
Нестабильный элемент, отсутствует в природе
102
No
НобелийНобелий
259,10
f-элемент
Нестабильный элемент, отсутствует в природе
103
Lr
ЛоуренсийЛоуренсий
266
f-элемент
Нестабильный элемент, отсутствует в природе
104
Rf
РезерфордийРезерфордий
267
6d2 7s2
Нестабильный элемент, отсутствует в природе
105
Db
ДубнийДубний
268
6d3 7s2
Нестабильный элемент, отсутствует в природе
106
Sg
СиборгийСиборгий
269
6d4 7s2
Нестабильный элемент, отсутствует в природе
107
Bh
БорийБорий
270
6d5 7s2
Нестабильный элемент, отсутствует в природе
108
Hs
ХассийХассий
277
6d6 7s2
Нестабильный элемент, отсутствует в природе
109
Mt
МейтнерийМейтнерий
278
6d7 7s2
Нестабильный элемент, отсутствует в природе
110
Ds
ДармштадтийДармштадтий
281
6d9 7s1
Нестабильный элемент, отсутствует в природе
Металлы
Неметаллы
Щелочные
Щелоч-зем
Благородные
Галогены
Халькогены
Полуметаллы
s-элементы
p-элементы
d-элементы
f-элементы
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
Горелка кислород пропан в Украине. Цены на Горелка кислород пропан на Prom.ua
Работает
Зварювальний пальник ГЗУ 248 пропан – кисень Донмет
На складе
Доставка по Украине
1 050 грн
Купить
Магазин “ГЕЛЕОС ПЛЮС”
Работает
ГЗУ Донмет 248 6/6 Горелка для высокотемпературной пайки пропаном черных и цветных металлов ,типа ГЗУ
Доставка из г. Харьков
1 131 грн
Купить
Интернет-магазин Ассорти Инструмент
Работает
ГЗУ «ДОНМЕТ» 247 (9/9) (пропан/кислород)
Доставка по Украине
1 145 грн
Купить
СВАРМАСТЕР
Работает
ГЗУ «ДОНМЕТ» 249 (пропан/кислород) или (МАФ)
Доставка по Украине
1 615 грн
Купить
СВАРМАСТЕР
Работает
ГЗУ «ДОНМЕТ» 262 (пропан/кислород) L-750мм
Доставка по Украине
2 795 грн
Купить
СВАРМАСТЕР
Работает
ГЗУ «ДОНМЕТ» 262 (пропан/кислород) L-1150мм
Доставка по Украине
3 113 грн
Купить
СВАРМАСТЕР
Работает
Горелка пропановая ГЗУ 228 ДОНМЕТ
Доставка по Украине
979. 20 грн
20 грн
Купить
Сваркомплект
Работает
ГЗУ ДОНМЕТ 247 9-9/6-6 Горелка однопламенная универсальная для газокислородной сварки,пайки,подогрева типа ГЗУ
Доставка из г. Харьков
1 253 грн
Купить
Интернет-магазин Ассорти Инструмент
Работает
ГЗУ ДОНМЕТ 249 Ф9 Горелка однопламенная универсальная для газокислородной сварки,пайки и подогрева типа ГЗУ
Доставка из г. Харьков
1 577 грн
Купить
Интернет-магазин Ассорти Инструмент
Работает
ГЗУ ДОНМЕТ 284 Micro 6/6 Горелка однопламенная универсальная для газокислородной пайки и подогрева тип ГЗМ
Доставка из г. Харьков
1 109 грн
Купить
Интернет-магазин Ассорти Инструмент
Работает
ГЗУ ДОНМЕТ 228 П 6/6 Горелка однопламенная универсальная для газокислородной сварки пайки и подогрева типа ГЗУ
Доставка из г. Харьков
980 грн
Купить
Интернет-магазин Ассорти Инструмент
Работает
ДОНМЕТ 206-01 JEWELLER Горелка однопламенная универсальная для газокислородной пайки и нагрева (ЮВЕЛИРНАЯ)
Доставка из г. Харьков
Харьков
1 599 грн
Купить
Интернет-магазин Ассорти Инструмент
Работает
Горелка для сварки H01-6C (кислородно-пропановая)
Доставка по Украине
554 грн
Купить
OOO “Поларис – ЭКО”
Работает
Горелка для сварки H01-2 (кислородно-пропановая)
Доставка по Украине
386 грн
Купить
OOO “Поларис – ЭКО”
Работает
ДОНМЕТ 206-02 JEWELLER Горелка однопламенная универсальная для газокислородной пайки и нагрева (ЮВЕЛИРНАЯ)
Доставка из г. Харьков
2 535 грн
Купить
Интернет-магазин Ассорти Инструмент
Смотрите также
Работает
ГЗУ “ДОНМЕТ” 262 L-750мм
Доставка по Украине
2 988 грн
Купить
Интернет-магазин Ассорти Инструмент
Работает
Сварочная горелка на МАПП-Газе VIVO HOME TS8000 КИТАЙ Оригинал с пьезоподжигом
Доставка по Украине
2 437.76 грн
Купить
интернет-магазин «VAVILON»
Работает
Горелка HT-2 для пайки (MAПП газ)
Доставка по Украине
2 306. 15 грн
15 грн
Купить
интернет-магазин «VAVILON»
Работает
Сварочная горелка (мапп газ) НТ- 1S660 с пьезоподжигом
Доставка по Украине
1 930.77 грн
Купить
интернет-магазин «VAVILON»
Работает
Сварочная горелка МАРР газ RTM – 1S660 с пьезоподжигом
Доставка по Украине
2 098.42 грн
Купить
интернет-магазин «VAVILON»
Работает
Сварочная горелка RTM 3660T пьезо МАР газ
Доставка по Украине
3 823.65 грн
Купить
интернет-магазин «VAVILON»
Работает
Газовые баллоны для горелок под МАПП-газ (MAPP GAS)
Доставка по Украине
757.25 грн
Купить
интернет-магазин «VAVILON»
Работает
Горелка газовая (газовоздушная-пропан) XTLine PA 23510
Доставка по Украине
1 054.37 грн
Купить
интернет-магазин «VAVILON»
Работает
Горелка газовая (газовоздушная-пропан) MAR-POL
Доставка по Украине
909.30 грн
Купить
интернет-магазин «VAVILON»
Работает
Набор газовых горелок MAYA
Доставка по Украине
372. 89 грн
89 грн
Купить
интернет-магазин «VAVILON»
Работает
Горелка пропан 72сm ( диаметр 5 mm) с клапаном пьезоподжиго, латунь
Доставка по Украине
875.90 грн
Купить
интернет-магазин «VAVILON»
Работает
Горелка пропан 73сm ( диаметр 5 mm) с пьезоподжигом, латунь
Доставка по Украине
567.81 грн
Купить
интернет-магазин «VAVILON»
Работает
Горелка пропан 97сm ( диаметр 8 mm)
Доставка по Украине
846.49 грн
Купить
интернет-магазин «VAVILON»
Работает
Горелка пропан 30″ ( диаметр 3 см) с клапаном
Доставка по Украине
249.76 грн
Купить
интернет-магазин «VAVILON»
Надежный партнер в вопросах поставки жидкого азота, кислорода и аргона в Поволжье. Оптовые Цены
КРИОГАЗПЛЮС – Надежный партнер в вопросах поставки жидкого азота, кислорода и аргона в Поволжье. Оптовые ЦеныХотите приобрести Технические газы?
Оставьте заявку – мы перезвоним и проконсультируем
Купить
ПОЧЕМУ ВЫГОДНЕЕ КУПИТЬ ТЕХНИЧЕСКИЕ ГАЗЫ У НАС
ГОСТ
РАБОТАЕМ КАК ЧАСЫ
ЛИЧНЫЙ АВТОПАРК
Газ пропан (C3H8) ГОСТ 20448-90
Пропан – Пропан – это бесцветный газ, который растворяется в большинстве органических растворителях. Не имеет запаха и цвета, ядовит. Конденсация происходит при температуре +25С, что позволяет транспортировать его в жидком состоянии. Хотя данное вещество невзрывоопасно, но смешавшись с воздухом, может воспламениться. Сгорает практически без остатка. Подразделяется на летний и зимний состав в процентном содержании. Для промышленных целей этот технический газ получают из нефтепродуктов.
Не имеет запаха и цвета, ядовит. Конденсация происходит при температуре +25С, что позволяет транспортировать его в жидком состоянии. Хотя данное вещество невзрывоопасно, но смешавшись с воздухом, может воспламениться. Сгорает практически без остатка. Подразделяется на летний и зимний состав в процентном содержании. Для промышленных целей этот технический газ получают из нефтепродуктов.
ПОЛУЧИТЬ КОНСУЛЬТАЦИЮ
Газ аргон (Ar2) в баллонах. ГОСТ 10157-79
Аргон – Газ аргон – технический газ, который нашел широкое применение в производстве. Он инертен, не имеет цвета и запаха. При нормальных условиях газ, при температуре минус 185 градусов Цельсия — жидкость. Не оказывает негативного воздействия на окружающую среду. Его часто используют на производствах, работающих с металлами. Аргоновая среда выступает в качестве защиты при сварке или резке металлов.
ПОЛУЧИТЬ КОНСУЛЬТАЦИЮ
Газ азот (N2) ГОСТ 9293-74
Азот – Азот является наиболее востребованным в промышленном производстве техническим газом. Особенности использования данного газа связаны с его физико-химическими свойствами. Это инертный газ, не имеющий цвета и запаха. Он нетоксичен для окружающей среды и человека. Очень часто его используют при сварке или высокотемпературной резке металлов, консервации трубопроводов. В медицине данным газом заполняют внутреннюю полость ртутного термометра. В жидком состоянии он является отличным хладагентом. Так же данный технический газ выступает компонентом оптических генераторов.
Особенности использования данного газа связаны с его физико-химическими свойствами. Это инертный газ, не имеющий цвета и запаха. Он нетоксичен для окружающей среды и человека. Очень часто его используют при сварке или высокотемпературной резке металлов, консервации трубопроводов. В медицине данным газом заполняют внутреннюю полость ртутного термометра. В жидком состоянии он является отличным хладагентом. Так же данный технический газ выступает компонентом оптических генераторов.
ПОЛУЧИТЬ КОНСУЛЬТАЦИЮ
Газ ацетилен (С2Н2) ГОСТ 5457-75
Ацетилен – Ацетилен – это химическое соединение широко используемое в промышленности. На сегодняшний день газ ацетилен в баллонах активно используется при автогенной сварке. Нельзя забывать о том, что разные марки данного вещества предназначены для различных целей. Для примера, баллоны марки «А» применяются в работе осветительной техники, а баллоны марки «В» идеально подходят при газопламенной обработке металлов. Но следует заметить, что в данной области у газа имеется более дешевый конкурент, а именно пропан-бутан.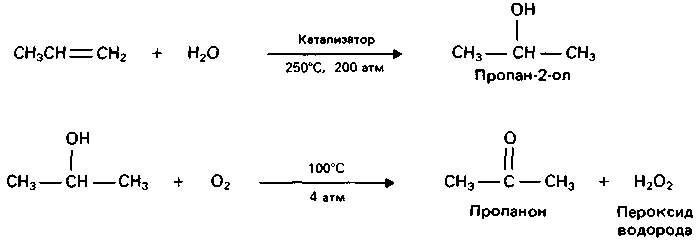 Несмотря на это опытные газосварщики, которые ведут работу в самых высоких температурных режимах, знают, что только этот газ имеет наиболее высокую температуру горения в сравнении с пропаном.
Несмотря на это опытные газосварщики, которые ведут работу в самых высоких температурных режимах, знают, что только этот газ имеет наиболее высокую температуру горения в сравнении с пропаном.
ПОЛУЧИТЬ КОНСУЛЬТАЦИЮ
Газ кислород (О2) в баллонах ГОСТ 5583-78
Кислород – За счет ярко выраженных окислительных свойств, кислород является наиболее востребованным техническим газом практически на каждом производстве. Невозможно представить металлургическую, пищевую, газовую промышленность без использования его. Ведь без него невозможен процесс горения. Кислород – это газ, который не имеет ни цвета, ни запаха, тяжелее воздуха. Он не токсичен, а значит, безопасен для окружающей среды. Но сильные концентрации кислорода могут вызвать воспламенение некоторых материалов. При взаимодействии со смазочными материалами взрывается. Температура кипения минус 183,0 градусов С, температура плавления минус 218,0 градусов С.
ПОЛУЧИТЬ КОНСУЛЬТАЦИЮ
ПОЯВИЛИСЬ ВОПРОСЫ? ПОЗВОНИТЕ НАМ ПРЯМО СЕЙЧАС
+7 (937) 526 99 05
ЗАДАТЬ ВОПРОС
ДОПОЛНИТЕЛЬНОЕ ОБОРУДОВАНИЕ
АЗОТНЫЙ КРИОДЕСТРУКТОР
КРИОФЕН
СОСУДЫ ДЮАРА
Наши друзья и партнеры
Благодаря тесным связям с нашими партнерами мы предлагаем Вам лучшее качество и самые “замороженные” цены. И это правильно.
И это правильно.
ПОЯВИЛИСЬ ВОПРОСЫ? ПОЗВОНИТЕ НАМ ПРЯМО СЕЙЧАС
+7 937 526 99 05
ЗАДАТЬ ВОПРОС
О Нас
Миссия сотрудников “КриоГазПлюс” уже на протяжении более 8 лет – это служение здоровью человека. Наш главный постулат – не навреди. Наши специалисты нацелены в первую очередь на помощь людям. Мы поддерживаем свою репутацию на высоком уровне и работаем с каждым нашим гостем сугубо индивидуально, в соответствии с его личными потребностями.
Полезная информация
КриоГазПлюс – это надежность и высочайшее качество. Всегда.
- Понедельник – Суббота, 9.00 – 19.30
- +7 937 526 99 05
- [email protected]
Мы ждем Вас по адресу
РТ, г. Казань, ул. Закиева д. 4.
Поделиться сайтом в сети
Пропан взаимодействует с кислородом в реакции горения при сварочных работах
Физико-технические особенности сварочных газов
Нефтеуглеводороды, в частности, пропан, бутан и их смеси, ацетилен, а также водород нашли широкое применение в различных сферах производства в качестве основных и вспомогательных соединений. Различные газы успешно используются как в качестве источников тепловой энергии, так и хладагентов. Одним из направлений их применения является сварочное дело и резка металла. Выбор газа в основном зависит от требуемой температуры сгорания.
Различные газы успешно используются как в качестве источников тепловой энергии, так и хладагентов. Одним из направлений их применения является сварочное дело и резка металла. Выбор газа в основном зависит от требуемой температуры сгорания.
Пропан и пропан-бутановые смеси
Углеводородные газы из группы алканов используются в тех случаях, когда нет необходимости в слишком высокой температуре газопламенной обработки: сварка тонкой стали и легкоплавких металлов, кислородная резка, пайка припоями и др. Пропан и бутан – это неядовитые и достаточно инертные газы, получаемые в качестве побочных продуктов при переработке нефти. При определенных условиях они взаимодействуют с кислородом, азотной кислотой и диоксидом азота, галогенами. При низкой температуре (-42 °С для пропана, -0,5 °С для бутана) и высоком давлении переходят в жидкое состояние.
Чаще всего используются пропан-бутановые смеси в соотношении 3:7 соответственно. Они обладают повышенной теплотворной способностью, а тепловая мощь сгорания в кислороде эффективнее, чем у ацетилена, но из-за небольшой скорости, с которой распространяется пламя, температура пламени меньше. В случае утечки газы скапливаются внизу помещения и могут, что может привести к образованию взрывоопасных концентраций.
В случае утечки газы скапливаются внизу помещения и могут, что может привести к образованию взрывоопасных концентраций.
Ацетилен
Ацетилен относится к ненасыщенным углеводородам, чем обусловлена его химическая активность. Соединение вступает в многочисленные реакции присоединения, цикломеризации, димеризации, окисления. Отличается резким запахом. Температура сжижения около -82 °С. При его сгорании требуется больше кислорода, чем для пропана и бутана. Для ацетилена свойственна высокая интенсивность горения, которая снижается при наличии в нем побочных веществ.
Водород
В промышленности газ получают различными способами: железопаровым, электролизом, конверсией. В зависимости концентрация чистого вещества находится в пределах 95 – 99,8 об. %. Температура сжижения -252 °С. Используется при кислородной разделительной резке в присутствии воды, сварке свинца, безокислительной пайке стали.
Технические характеристики газов: сравнительная таблица
|
Параметр |
Пропан-бутановая смесь |
Ацетилен |
Водород |
|
Плотность при температуре 20 °С и давлении 0,1 МПа, кг/м3 |
2,21 |
1,091 |
0,084 |
|
Температура воспламенения в кислороде, °С |
500 |
240-630 |
510 |
|
Низшая теплотворная способность, кДж/м3 |
88800 |
52800 |
10800 |
|
Скорость распространения пламени в смеси с кислородом, м/с |
4,5 |
13,5 |
– |
Меры безопасности
В связи с большой взрывоопасностью сварочных газов предъявляются особые требования к условиям и помещениям проведения работ, хранению газовых баллонов. Особое внимание уделяется отсутствию источников возникновения пламени, искры, легковоспламеняющихся веществ. Помещения оборудуются специальными осветительными приборами, системами вентиляции и кондиционирования. Сварочные работы проводятся в присутствии более двух человек при обязательном оформлении наряда-допуска.
Особое внимание уделяется отсутствию источников возникновения пламени, искры, легковоспламеняющихся веществ. Помещения оборудуются специальными осветительными приборами, системами вентиляции и кондиционирования. Сварочные работы проводятся в присутствии более двух человек при обязательном оформлении наряда-допуска.
Каталог технических газов от нашей компании
Кислород
Углекислота
Ацетилен
Азот
Аргон
Гелий
Пропан
Сварочная смесь
Отличительная окраска газовых баллонов
Отличительная окраска газонаполненных баллонов малой, средней и большой емкости отечественного производства (ГОСТ 949-73, ГОСТ 12247-80, ТР ТС 032/2013) и зарубежных производителей (EN 1089-3)
ГОСТ 949-73
| Газ | Цвет баллона | Цвет надписи | Цвет полосы | Пример |
| Азот | Чёрный | Жёлтый | Коричневый | Азот
|
| Аммиак | Жёлтый | Черный | – | Аммиак |
| Аргон сырой | Чёрный | Белый | Белый | Аргон сырой
|
| Аргон технический | Чёрный | Синий | Синий | Аргон технический
|
| Аргон чистый | Серый | Зелёный | Зелёный | Аргон чистый
|
| Ацетилен | Белый | Красный | – | Ацетилен |
| Бутилен | Красный | Жёлтый | Чёрный | Бутилен
|
| Водород | Тёмно-зелёный | Красный | – | Водород |
| Гелий | Коричневый | Белый | – | Гелий |
| Закись азота | Серый | Чёрный | – | Закись азота |
| Кислород | Голубой | Чёрный | – | Кислород |
| Кислород медицинский | Голубой | Чёрный | – | Кислород медицинский |
| Нефтегаз | Серый | Красный | – | Нефтегаз |
| Сернистый ангидрид | Чёрный | Белый | Жёлтый | Сернистый ангидрид
|
| Сероводород | Белый | Красный | Красный | Сероводород
|
| Сжатый воздух | Чёрный | Белый | – | Сжатый воздух |
| Углекислота | Чёрный | Жёлтый | – | Углекислота |
| Фосген | Защитный | – | Красный | Фосген
|
| Фреон-11 | Серебристый | Чёрный | Синий | Фреон-11
|
| Фреон-12 | Серебристый | Чёрный | – | Фреон-12 |
| Фреон-13 | Серебристый | Чёрный | Две красных | Фреон-13
|
| Фреон-22 | Серебристый | Чёрный | Две жёлтых | Фреон-22
|
| Хлор | Защитный | – | Зелёный | Хлор
|
| Циклопропан | Оранжевый | Чёрный | – | Циклопропан |
| Этилен | Фиолетовый | Красный | – | Этилен |
| Все остальные горючие газы | Красный | Белый | – | Газ |
| Все остальные негорючие газы | Чёрный | Жёлтый | – | Газ |
EN 1089-3
| Газ |
Цвет баллона RAL |
Пример |
| Кислород дыхательный | Зеленый RAL 6035 | |
| Кислород | Белый RAL 9010 | |
| Азот | Черный RAL 9005 | > |
| Закись азота | Темно-синий RAL 5010 | |
| Гелий | Коричневый RAL 8008 | |
| Ядовитый и/или коррозионный газ | Желтый RAL 1018 | |
| Легковоспламеняющийся газ | Красный RAL 3000 | |
| Окисляющий газ | Голубой RAL 5012 | |
| Удушающий инертный газ | Светло-зеленый RAL 6018 |
Сигнал-033.
 Снят с производства. Замена Сигнал-03.
Снят с производства. Замена Сигнал-03.- До 4 измерительных каналов
- Выносные датчики, линия связи до 1км
- Интерфейсы RS-485 (ModBus RTU), USB 2.0
- Релейные выходы
- Цифровая индикация
- Световая и звуковая сигнализация
Газоанализаторы-сигнализаторы СИГНАЛ-033 предназначены для измерения концентраций взрывоопасных и токсичных газов в атмосферном воздухе с подачей аварийной сигнализации при превышении концентрации контролируемого газа заданного уровня в окружающем воздухе. Это метан, пропан, кислород, (в объемных доля процента), оксид углерода и аммиак (в миллиграмм на метр в кубе).
Сигнализатор представляет собой двухблочный стационарный газоанализатор непрерывного действия с диффузионной подачей газа.
Сигнализатор состоит из автономного измерительного блока БКУ и выносных датчиков МИГ (модульных измерителей газа).
Измерительный блок (БКУ), по заказу потребителя, может дополнительно оснащаться ЖК – индикатором для индикации показаний датчиков, модулем силовых реле для управления внешними исполнительными устройствами и блоком гальванической развязки питания датчиков.
Функции БКУ:
- Преобразование аналогового сигнала датчиков в цифровой, отображение на ЖК индикаторе измеряемой концентрации газов и состояния датчиков;
- Формирование звуковых световых сигналов превышения установленных пороговых значений;
- Формирование сигналов на срабатывания «сухих» контактов силовых реле;
- Запись и хранение в энергонезависимой памяти аварийных событий, неисправности оборудования и сбоев в энергоснабжении сигнализатора;
- Формирование сигналов управления с внешними устройствами по интерфейсу RS-485.
Датчики серии МИГ предназначены для преобразования концентрации измеряемого газового компонента в электрический токовый сигнал:
- Датчики с электрохимическим сенсором (МИГ-ЭЛ) для преобразования концентраций паров аммиака, оксида углерода и кислорода;
- Датчики с термокаталитическим сенсором (МИГ-ТК) для преобразования концентраций метана и пропана;
- Датчики с оптико-абсорбционным преобразователем (далее по тексту МИГ-ОП) для преобразования концентраций метана и пропана.

Датчики серии МИГ на метан, пропан, кислород, аммиак и оксид углерода выполняются в силуминовом и пластиковом корпусах.
По заявке потребителя, для датчиков метана и пропана возможно исполнение датчиков для рабочих температур до минус 40°С с диапазоном показаний до 100 % НКПР или до минус 10°С с диапазоном показаний до 50 % НКПР.
Для датчиков аммиака и оксида углерода возможно исполнение датчиков для температур до минус 30°С или до минус 10°С.
Газоанализаторы могут использоваться как автономно, так и в составе измерительных систем.
Технические характеристики
| Параметр | Значение |
|---|---|
| Число каналов | 1-4 |
| Максимальная удаленность датчиков | от пульта до 1 км двухпроводной линией |
| Число встроенных реле | 4 |
| Принцип измерения | Термокаталитический, электрохимический, оптический |
| Выход | световая и звуковая индикация, реле «сухие контакты» |
| Число порогов сигнализации | 1-3 |
| Звуковая и световая сигнализация | для каждого порога при превышении установленных пороговых значений |
| Электропитание | 220В, 50 Гц |
| Потребляемая мощность, не более: – в режиме измерения – в аварийном режиме измерения |
25 ВА 30 ВА |
| Ток короткого замыкания (Ех) | не более 180 мА |
| Выходное постоянное напряжение искробезопасных источников питания | не более 25,6 В |
| Внешние интерфейсы | RS-485 (ModBus RTU) USB 2.  0 0 |
| Коммутационные параметры реле | MAX: 2А, 150В |
| Электрическое сопротивление изоляции контактов датчика, «сухих контактов» реле и контактов интерфейса RS-485 относительно контактов подключения электропитания, МоМ, не менее: | 20 |
| Энергонезависимая память | да |
| Архивация событий | да |
| Маркировка взрывозащиты | Пульт [Exib]IIB Датчик 1ExibdllBT4 X |
| Степень защиты от внешних воздействий | Пульт IP20 Датчик IP54 |
| Рабочая температура | Пульт -5°С … +40°С Датчик -40°С … +50°С |
| Габариты | Пульт 216мм х 247мм х 117мм Датчик(силумин) 109мм х 118мм х 54мм Датчик(пластик) 130мм х 112мм х 66мм |
| Масса, не более | Пульт 2,0 кг Датчик МИГ (силумин) 0,6 кг Датчик МИГ (пластик) 0,3 кг |
| Периодичность поверки | 12 месяцев |
| Средняя наработка на отказ газоанализатора, ч, не | 10000 |
| Средний срок службы, лет, не менее | 10 при условии своевременного проведения предписанных ТУ регламентных работ. |
Характеристики датчиков
| Параметр | МИГ-ТК-Ch5 | МИГ-ТК-С3Н8 | МИГ-ОП-СН4 | МИГ-ОП-С3Н8 | МИГ-ЭЛ-О2 | МИГ-ЭЛ-СО-ECO, МИГ-ЭЛ-СО -AF | МИГ-ЭЛ-Nh4-MR1000, МИГ-ЭЛ-Nh4-PL1000 |
|---|---|---|---|---|---|---|---|
| Измеряемый газ | Метан | Пропан | Метан | Пропан | Кислород | Оксид углерода | Аммиак |
| Диапазон измерений | 15 – 50 % НКПР | 15 – 50 % НКПР | 14 – 22 об.д. % | 0 – 250 мг/м3 | 0 – 500 мг/м3 | ||
| Диапазон показаний | 0 – 50 % НКПР | 0 – 100 % НКПР | 1 – 22 об. д. % д. % |
0 – 300 мг/м3 | 0 – 710 мг/м3 | ||
| Пределы допускаемой основной абсолютной погрешности | ±5 % НКПР | ±1 об. доля, % | – | – | |||
| Приведенная погрешность | – | – | ±25 % в диапазоне от 0 до 110 мг/м3 |
±25 % в диапазоне от 0 до 165 мг/м3 |
|||
| Относительная погрешность | – | – | ±25 % в диапазоне от 110 до 250 мг/м3 |
±25 % в диапазоне от 165 до 500 мг/м3 |
|||
| Время прогрева, мин | 15 | 30 | 15 | 30 | |||
| Время установления показаний Т90, с | 30 | 30 | 60 | 20мин. |
|||
| Предел допускаемой дополнительной погрешности от изменения температуры окружающего воздуха на каждые 10°С от нормальной температуры (20°С), доля основной погрешности | 0.5 | 0.5 | 0.5 | ||||
| Значения содержаний измеряемого компонента на установленных порогах срабатывания сигнализации | 10 и 20 (% НКПР) |
18 (об. доля, %) |
20 и 100 (мг/м3) |
20, 60, 500 (мг/м3) |
|||
Условия эксплуатации
| Наименование блока | Параметры | ||
|---|---|---|---|
| Температура окружающей среды, °C | Атмосферное давление, кПа | Относительная влажность, % | |
| БКУ | от минус 20 до плюс 40 | от 84 до 106,7 | от 30 до 80 |
| МИГ-ТК-СН4 | от минус 10 до плюс40 | ||
| МИГ-ТК-С3Н8 | от минус 10 до плюс40 | ||
| МИГ-ОП-СН4 | от минус 40 до плюс 50 | ||
| МИГ-ОП-С3Н8 | от минус 40 до плюс 50 | ||
| МИГ-ЭЛ-О2 | от минус 30 до плюс 55 | ||
| МИГ-ЭЛ-СО-ECO | от минус 10 до плюс 50 | ||
| МИГ-ЭЛ-СО-AF | от минус 30 до плюс 50 | ||
| МИГ-ЭЛ-Nh4-MR1000 | от минус 10 до плюс 50 | ||
| МИГ-ЭЛ-Nh4-PL1000 | от минус 30 до плюс 50 | ||
Режимы работы датчиков
| Режим работы | Индикация | Примечание | ||
|---|---|---|---|---|
| “Питание” | “Сбой” | “Порог” | ||
| Рабочие режимы датчика | ||||
| Работа | + | – | – | Постоянное свечение |
| Неисправность | – | + | – | См. руководство по эксплуатации руководство по эксплуатации |
| Превышение предупредительного порога (только для МИГ-ОП) | – | – | + | Импульсное свечение с частотой 0.5 Гц |
| Превышение аварийного порога | – | – | + | Постоянное свечение |
| Настроечные режимы датчика | ||||
| Прогрев сенсора при включении | – | + | – | Импульсное свечение с частотой 0.5 Гц |
| Установка нуля датчика (значения 21% об. для МИГ-ЭЛ-О2) | + | + | – | См. руководство по эксплуатации |
Габаритные размеры
Габаритные размеры БКУ с установленной DIN-рейкой:
Габаритные и присоединительные размеры датчиков МИГ:
Комплект поставки
| Наименование | Количество | |
|---|---|---|
| Блок индикации | БКУ | 1 |
| DIN-рейка | 1 | |
| Датчик | МИГ-ТК | По заказу |
| МИГ-ОП | По заказу | |
| МИГ-ЭЛ | По заказу | |
| Соба крепления пластиковых датчиков серии МИГ | По заказу | |
| Предохранитель ВП1-1 2,0А | 2 | |
| Приспособление для поверки МИГ-ТК | По заказу | |
| Приспособление для поверки МИГ-ЭЛ, -ОП | По заказу | |
Руководство по эксплуатации ГКПС 63. 00.00.000РЭ 00.00.000РЭ |
1 | |
| Разъем 2РМ14КПН4Г1В1 | По заказу | |
| Ключ аппаратной перезагрузки БКУ | 2 | |
Примечание: Силовой кабель питания БКУ, кабели связи датчиков с БКУ в комплектацию не входят.
Пропан (C3H8)
Пропан представляет собой трехуглеродный алкан, обычно газ, но его можно сжимать до транспортируемой жидкости. Его получают из других нефтепродуктов при переработке нефти или природного газа. Он обычно используется в качестве топлива для двигателей, газокислородных горелок, барбекю, переносных печей и центрального отопления жилых помещений.
При использовании в качестве автомобильного топлива он широко известен как сжиженный нефтяной газ (LPG или LP-gas), который может представлять собой смесь пропана с небольшими количествами пропилена, бутана и бутилена. Также добавляется отдушка этантиол, чтобы люди могли легко почувствовать запах газа в случае утечки.
Его название произошло от части «пропионовой кислоты» (которая также имеет 3 атома углерода) и суффикса -ан.
Свойства и реакции
Пропан подвергается реакциям горения аналогично другим алканам. В присутствии избытка кислорода пропан сгорает с образованием воды и углекислого газа.
- C 3 H 8 + 5 O 2 → 3 CO 2 + 4 H 2 O + тепло
Пропан + кислород → углекислый газ + вода
Когда кислорода недостаточно для полного сгорания, происходит неполное сгорание, когда пропан сгорает и образует воду, монооксид углерода, диоксид углерода и углерод.
- C 3 H 8 + 3,5 O 2 → CO 2 + CO + C + 4 H 2 O + тепло
Пропан + Кислород → Углекислый газ + Угарный газ + Углерод + Вода
В отличие от природного газа пропан тяжелее воздуха (в 1,5 раза плотнее). В сыром виде пропан тонет и скапливается на полу.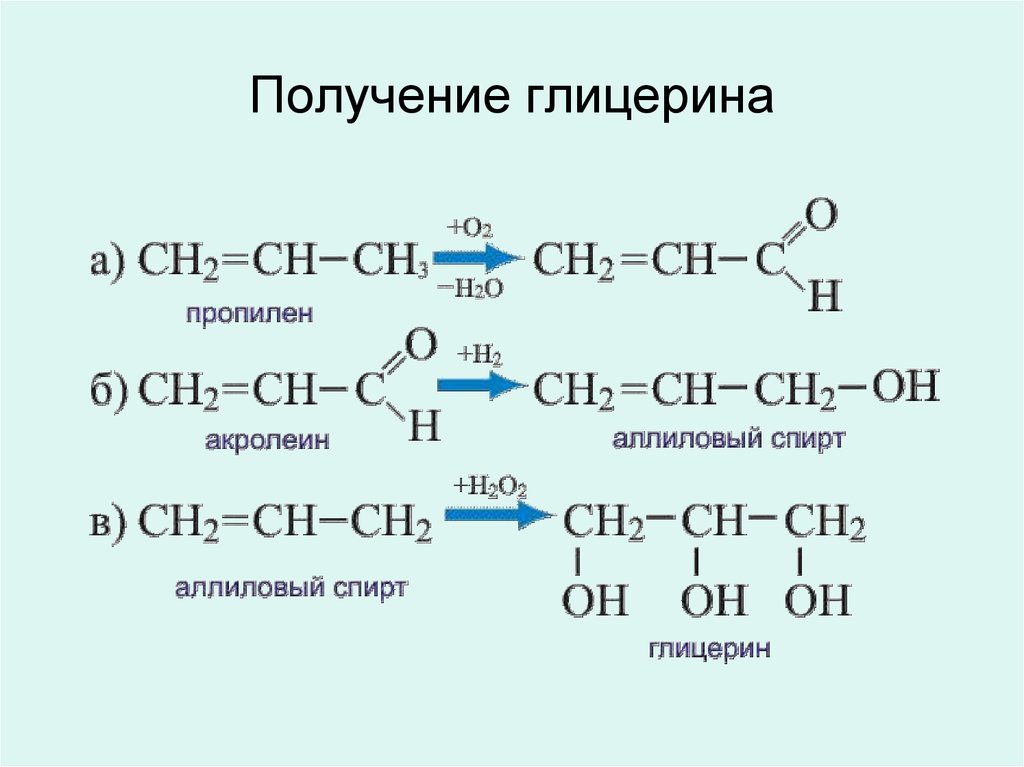 Жидкий пропан испаряется при атмосферном давлении и выглядит белым из-за конденсации влаги из воздуха.
Жидкий пропан испаряется при атмосферном давлении и выглядит белым из-за конденсации влаги из воздуха.
При правильном сгорании пропан производит около 50 МДж/кг. Полная теплота сгорания одного нормального кубического метра пропана составляет около 91 мегаджоуля
Пропан нетоксичен; однако при злоупотреблении в качестве ингалятора он представляет небольшой риск удушья из-за кислородного голодания. Коммерческие продукты содержат углеводороды помимо пропана, что может увеличить риск. Обычно хранящийся под давлением при комнатной температуре, пропан и его смеси расширяются и охлаждаются при выпуске и могут вызвать легкое обморожение.
Сжигание пропана намного чище, чем сжигание бензина, хотя и не так чисто, как сжигание природного газа. Наличие связей С-С, а также множественные связи пропилена и бутилена создают органические выхлопы помимо углекислого газа и водяного пара при обычном сгорании. Эти связи также вызывают горение пропана видимым пламенем.
Коэффициенты выбросов парниковых газов для пропана составляют 62,7 кг CO 2 /мБТЕ или 1,55 кг CO 2 на литр или 73,7 кг/ГДж.
В отличие от природного газа пропан тяжелее воздуха (в 1,5 раза плотнее). В сыром виде пропан тонет и скапливается на полу. Жидкий пропан испаряется при атмосферном давлении и выглядит белым из-за конденсации влаги из воздуха.
При правильном сгорании пропан производит около 50 МДж/кг. Полная теплота сгорания одного нормального кубического метра пропана составляет около 91 мегаджоуля
Пропан нетоксичен; однако при злоупотреблении в качестве ингалятора он представляет небольшой риск удушья из-за кислородного голодания. Коммерческие продукты содержат углеводороды помимо пропана, что может увеличить риск. Обычно хранящийся под давлением при комнатной температуре, пропан и его смеси расширяются и охлаждаются при выпуске и могут вызвать легкое обморожение.
Сжигание пропана намного чище, чем сжигание бензина, хотя и не так чисто, как сжигание природного газа. Наличие связей С-С, а также множественные связи пропилена и бутилена создают органические выхлопы помимо углекислого газа и водяного пара при обычном сгорании. Эти связи также вызывают горение пропана видимым пламенем.
Эти связи также вызывают горение пропана видимым пламенем.
Коэффициенты выбросов парниковых газов для пропана составляют 62,7 кг CO 2 /мБТЕ или 1,55 кг CO 2 на литр или 73,7 кг/ГДж.
Использование Пропан используется в качестве топлива для приготовления пищи на многих барбекю, переносных плитах и в автомобилях. Вездесущий стальной контейнер объемом 4,73 галлона (20 фунтов) часто называют «танком для барбекю». Пропан остается популярным выбором для барбекю и переносных печей, потому что его низкая температура кипения -42 C (-43,6 F) заставляет его испаряться, как только он высвобождается из контейнера под давлением. Следовательно, не требуется карбюратор или другое испарительное устройство; достаточно простой дозирующей форсунки. Пропан приводит в действие некоторые локомотивы, автобусы, вилочные погрузчики, такси и машины для замены льда, а также используется для обогрева и приготовления пищи в транспортных средствах для отдыха и кемпингах. Во многих сельских районах Северной Америки пропан используется в печах, кухонных плитах, водонагревателях, сушилках для белья и других приборах, производящих тепло. В этом случае он обычно хранится в большом стационарном баллоне, который заправляется грузовиком для доставки пропана. По состоянию на 2000 г. 6,9миллионов американских домохозяйств используют пропан в качестве основного топлива для отопления.
Во многих сельских районах Северной Америки пропан используется в печах, кухонных плитах, водонагревателях, сушилках для белья и других приборах, производящих тепло. В этом случае он обычно хранится в большом стационарном баллоне, который заправляется грузовиком для доставки пропана. По состоянию на 2000 г. 6,9миллионов американских домохозяйств используют пропан в качестве основного топлива для отопления.
Имеющееся в продаже «пропановое» топливо, или сжиженный нефтяной газ, не является чистым. Как правило, в США и Канаде это в основном пропан (не менее 90%), остальное в основном бутан и пропилен (максимум 5%), а также отдушки. Это стандарт HD-5 (Heavy Duty — максимально допустимое содержание пропилена 5%), написанный для двигателей внутреннего сгорания. Сжиженный нефтяной газ при извлечении из природного газа не содержит пропилена. Сжиженный нефтяной газ при очистке от сырой нефти действительно содержит пропилен. Не все продукты с маркировкой «пропан» соответствуют этому стандарту. В Мексике, например, содержание бутана намного выше.
В Мексике, например, содержание бутана намного выше.
Бытовое и промышленное топливо
В Северной Америке местные грузовики для доставки, называемые «бобтейлами», со средним объемом бака 3000 галлонов, заполняют большие резервуары (иногда называемые скребками ), которые постоянно установлены на территории, или другие сервисные грузовики обменивают пустые баллоны с пропаном на заполненные цилиндры. Большие грузовики с тягачами, называемые «грузовыми лайнерами», со средним объемом бака 10 000 галлонов транспортируют пропан от трубопровода или нефтеперерабатывающего завода до местного завода по доставке. Бобтейл и транспорт не уникальны для рынка Северной Америки, хотя практика не так распространен в других местах, и транспортные средства обычно обозначаются как танкеры . Во многих странах пропан доставляется потребителям в индивидуальных цистернах малого или среднего размера.
Использование пропана быстро растет в неиндустриальных районах мира. Пропан заменяет древесину и другие традиционные источники топлива в таких местах, где его теперь иногда называют «газом для приготовления пищи». Североамериканские грили-барбекю, работающие на пропане, нельзя использовать за границей. «Пропан», продаваемый за границей, на самом деле представляет собой смесь пропана и бутана. Чем теплее страна, тем выше содержание бутана, обычно 50/50, а иногда и до 75% бутана. Использование откалибровано для насадок разного размера, используемых в грилях за пределами США. Американцы, которые берут свои грили за границу, например, военнослужащие, могут найти пропан, соответствующий требованиям США, на биржах военной почты AAFES.
Североамериканские грили-барбекю, работающие на пропане, нельзя использовать за границей. «Пропан», продаваемый за границей, на самом деле представляет собой смесь пропана и бутана. Чем теплее страна, тем выше содержание бутана, обычно 50/50, а иногда и до 75% бутана. Использование откалибровано для насадок разного размера, используемых в грилях за пределами США. Американцы, которые берут свои грили за границу, например, военнослужащие, могут найти пропан, соответствующий требованиям США, на биржах военной почты AAFES.
Промышленность Северной Америки, использующая пропан, включает производителей стекла, кирпичные печи, птицефабрики и другие отрасли, которым требуется портативное тепло.
Охлаждение
Пропан также играет важную роль в обеспечении автономного охлаждения, обычно с помощью абсорбционного холодильника.
Смеси чистого сухого «изопропана» (R-290a) (коммерческий термин, используемый для описания смесей изобутана/пропана) и изобутана (R-600a) обладают незначительным потенциалом разрушения озонового слоя и очень низким потенциалом глобального потепления и могут служить функциональной заменой R -12, R-22, R-134a и другие хлорфторуглеродные или гидрофторуглеродные хладагенты в обычных стационарных системах охлаждения и кондиционирования воздуха.
Такая замена широко запрещена или не рекомендуется в автомобильных системах кондиционирования воздуха на том основании, что использование легковоспламеняющихся углеводородов в системах, изначально предназначенных для работы с негорючим хладагентом, представляет значительный риск возгорания или взрыва.
Продавцы и защитники углеводородных хладагентов выступают против таких запретов на том основании, что таких инцидентов было очень мало по сравнению с количеством систем кондиционирования воздуха транспортных средств, заполненных углеводородами. Один конкретный тест был проведен профессором Университета Нового Южного Уэльса, который непреднамеренно проверил наихудший сценарий внезапной и полной утечки хладагента в салон с последующим воспламенением. Он и еще несколько человек в машине получили ожоги лица, ушей и рук, а несколько наблюдателей получили рваные раны от разбитого стекла окна переднего пассажира.
Автомобильное топливо
Пропан также все чаще используется в качестве автомобильного топлива. В США 190 000 дорожных транспортных средств используют пропан, а 450 000 вилочных погрузчиков используют его для питания. Это третье по популярности автомобильное топливо в Америке после бензина и дизельного топлива. В других частях мира пропан, используемый в автомобилях, известен как автогаз. Около 9 миллионов автомобилей по всему миру используют автогаз.
В США 190 000 дорожных транспортных средств используют пропан, а 450 000 вилочных погрузчиков используют его для питания. Это третье по популярности автомобильное топливо в Америке после бензина и дизельного топлива. В других частях мира пропан, используемый в автомобилях, известен как автогаз. Около 9 миллионов автомобилей по всему миру используют автогаз.
Преимуществом пропана является его жидкое состояние при умеренном давлении. Это обеспечивает быстрое время заправки, доступную конструкцию топливного бака и запас хода, сравнимый (хотя и меньший) с бензином. Между тем оно заметно чище (как при обращении, так и при сгорании), приводит к меньшему износу двигателя (из-за нагара), не разбавляет моторное масло (часто продлевая интервалы замены масла) и до недавнего времени было относительно выгодным предложением в Северной Америке. Октановое число заметно выше 110. Однако публичные заправочные станции все еще редкость. Многие переоборудованные автомобили имеют приспособления для дозаправки из «бутылок для барбекю». Специально построенные автомобили часто находятся в коммерческих автопарках и имеют частные заправочные станции.
Специально построенные автомобили часто находятся в коммерческих автопарках и имеют частные заправочные станции.
Пропан обычно хранится и транспортируется в стальных баллонах в виде жидкости с паровым пространством над жидкостью. Давление пара в цилиндре зависит от температуры. Когда газообразный пропан вытягивается с высокой скоростью, скрытая теплота испарения, необходимая для создания газа, приводит к охлаждению баллона. (Вот почему вода часто конденсируется на стенках бутылки, а затем замерзает). В экстремальных случаях это может привести к такому значительному снижению давления, что процесс больше не сможет поддерживаться. Кроме того, легкие высокооктановые смеси испаряются раньше, чем более тяжелые низкооктановые. Таким образом, свойства воспламенения изменяются по мере опустошения бака. По этим причинам жидкость часто отбирают с помощью погружной трубки.
Прочее
- Пропан используется в качестве исходного сырья для производства базовых нефтехимических продуктов при крекинге с водяным паром.

- Пропан используется в некоторых огнеметах в качестве топлива или в качестве нагнетающего газа.
- Некоторое количество пропана становится сырьем для пропилового спирта, обычного растворителя.
- Пропан является основным топливом для воздушных шаров.
- Используется в производстве полупроводников для осаждения карбида кремния.
- Пропан смешивается с силиконом для образования пропеллента (продается как зеленый газ), который используется для питания газовых пистолетов, используемых в боевых играх страйкбола.
- Жидкий пропан обычно используется в тематических парках и в киноиндустрии в качестве недорогого высокоэнергетического топлива для взрывов и других спецэффектов.
Пропан тяжелее воздуха. Если произойдет утечка в топливной системе пропана, газ будет иметь тенденцию просачиваться в любое замкнутое пространство и, таким образом, создавать риск взрыва и возгорания. Типичный сценарий — протекающий баллон, хранящийся в подвале; утечка пропана стекает по полу к запальнику печи или водонагревателя и приводит к взрыву или пожару.
Типичный сценарий — протекающий баллон, хранящийся в подвале; утечка пропана стекает по полу к запальнику печи или водонагревателя и приводит к взрыву или пожару.
Пропан покупается и хранится в жидкой форме (СНГ), поэтому энергия топлива может храниться в относительно небольшом пространстве. Сжатый природный газ (СПГ), в основном метан, является еще одним газом, используемым в качестве топлива, но его нельзя сжижать путем сжатия при нормальных температурах (которые намного выше критической температуры метана, и поэтому для хранения требуется очень высокое давление (что создает опасность, связанную с в случае аварии баллон с СПГ может взорваться с большой силой или достаточно быстро, чтобы превратиться в самоходную ракету). Следовательно, СПГ гораздо менее эффективно хранить из-за требуемого большого объема бака. Таким образом, пропан гораздо чаще используется для заправки транспортных средств. чем природный газ, и требуется всего 1220 килопаскалей (177 фунтов на кв. дюйм) давления, чтобы поддерживать его в жидком состоянии при температуре 37,8 C (100 F)9. 0003
0003
Уровень жидкости в баллоне с пропаном можно измерить с помощью внутреннего магнитного «поплавка». Затем внешний манометр может определять положение поплавка в резервуаре. Эта магнитная поплавковая система не может точно измерить общее количество пропана, поскольку газообразная часть пропана внутри резервуара не учитывается при измерении.
Самый точный способ измерить количество пропана, оставшегося в баллоне с пропаном, — это взвесить его. На боковой стороне бака должны быть выбиты буквы TW, за которыми следует цифра. Это число представляет собой вес пустого резервуара в фунтах или его собственный вес. Типичный баллон с пропаном на 5 галлонов может иметь собственный вес 10 фунтов. Если бы этот баллон весил 20 фунтов, то из этого следует, что в баллоне 9 хранится 10 фунтов пропана.0003
Галлон пропана содержит 91 690 БТЕ. Умножение этого числа на количество галлонов в баке дает 152 205 БТЕ тепловой энергии (1,66 91 690 = 152 205).
Затем можно рассчитать время работы конкретного устройства, если известно потребление БТЕ устройства. Это число, выраженное в БТЕ в час, обычно можно найти на приборе или у производителя. Продолжая этот пример, устройство, потребляющее 12 000 БТЕ в час, обеспечит 12,68 часов работы (152 205 12 000 ≈ 12,68).
ИсточникиПропан производится как побочный продукт двух других процессов: переработки природного газа и нефтепереработки.
Переработка природного газа включает удаление бутана, пропана и больших количеств этана из неочищенного газа для предотвращения конденсации этих летучих веществ в трубопроводах природного газа. Кроме того, нефтеперерабатывающие заводы производят некоторое количество пропана в качестве побочного продукта крекинга нефти в бензин или печное топливо.
Предложение пропана не может быть легко скорректировано с учетом возросшего спроса из-за того, что производство пропана является побочным продуктом. Около 90% пропана в США производится внутри страны.
Соединенные Штаты импортируют около 10% пропана, потребляемого каждый год, причем около 70% этого объема поступает из Канады по трубопроводу и по железной дороге. Остальные 30% импортируемого пропана поступают в США из других источников морским транспортом.
После производства североамериканский пропан хранится в огромных соляных пещерах, расположенных в форте Саскачеван, Альберта, Канада; Мон Бельвье, Техас и Конвей, Канзас. Эти соляные пещеры были выдолблены в 19 в.40s и может хранить до 80 миллионов баррелей пропана или больше. Когда пропан необходим, большая его часть транспортируется по трубопроводам в другие районы Среднего Запада, Севера и Юга для использования потребителями. Пропан также доставляется баржами и железнодорожными вагонами в некоторые районы США.
Пропан неполное + полное сгорание
- администратор
- Последнее обновление: 27 июля 2021 г.
Полное сгорание пропана (СНГ) имеет важное значение. Полное сгорание сжиженного нефтяного газа экономит ваши деньги на газе.

Уравнение пропана для полного сгорания пропана включает в себя пропан и кислород в качестве входного топлива, а также двуокись углерода, воду, тепло и, возможно, монооксид углерода в качестве выходов. Полное сгорание СНГ – пропана – дает около 25 МДж/л или 49 МДж/кг тепла.
Неполное сгорание приводит к образованию угарного газа, который является ядовитым газом.
Узнайте, что вам нужно сделать…
При сжигании сжиженного нефтяного газа образуется угарный газ – Выделяется ли сжиженный газ угарный газ
Приборы, работающие на природном газе или пропане (СНГ), могут выделять угарный газ при сгорании с неполным сгоранием. Правильно работающие газовые приборы производят мало угарного газа, если вообще производят его.
Неполное и полное сгорание пропана
Пропан – сжиженный нефтяной газ – горит в пределах своей воспламеняемости.
Нижний и верхний пределы воспламеняемости представляют собой процентное содержание СНГ в смеси СНГ/воздух.
Это означает, что от 2,15 % до 9,6 % всей смеси LPG/воздух должен составлять LPG, чтобы он был горючим.
Однако оптимальной смесью является 4% LPG/воздух.
Итак, 4 части сжиженного нефтяного газа (пропана) на 96 частей воздуха.
При полном сгорании пропана горелка дает голубое пламя с тепловыделением около 25 МДж/л или 49 МДж/кг.
Таким образом, более богатые смеси, близкие к 9,6%, скорее всего, будут страдать от неполного сгорания.
Желтое пламя, сажа и чрезмерная конденсация являются тремя физическими признаками неполного сгорания.
Природный газ – метан – пределы воспламенения разные, от 5,4% до 17%.
Оптимальная горючая смесь для метана тоже другая, примерно 10,42%.
Уравнение полного сгорания пропана – формула сгорания для сжиженного нефтяного газа
В уравнении полного сгорания пропана в присутствии достаточного количества кислорода пропан сгорает с образованием водяного пара и углекислого газа, а также дает около 25 МДж/л или 49 МДж/кг тепла. Итак, это уравнение полного сгорания пропана как в словах, так и в химических формулах:
Итак, это уравнение полного сгорания пропана как в словах, так и в химических формулах:
Пропан + Кислород → Углекислый газ + Вода + Теплота (около 25 МДж/л или 49 МДж/кг)
C 3 H8 + 5 O 2 → 3 CO 2 + 4 H 2 O + Теплота
Уравнение неполного сгорания пропана-сжиженного нефтяного газа
Уравнение неполного сгорания пропана: 9 O3H8 + 9 O2H8 + 4 СО2 + 2 СО + 8 ч3О + Тепло.
Если кислорода недостаточно для полного сгорания, происходит неполное сгорание.
Результатом неполного сгорания снова являются водяной пар, углекислый газ и тепло.
Но он также производит окись углерода.
Уравнение неполного сгорания пропана-СНГ в словах и символах
Газ + Кислород = Вода + Двуокись углерода + Окись углерода + Тепло
2 C 3 H 8 + 9 O 8 2 CO 2 + 2 CO + 8 H 2 O + Тепло
Неполное сгорание с образованием угарного газа
Угарный газ – CO – ядовитый газ.
Приборы, работающие на природном или пропановом (СНГ), могут выделять окись углерода с неполным сгоранием.
Правильно работающие газовые приборы производят мало угарного газа, если вообще производят.
Горение и угарный газ (СО) – продукты, образующиеся при сжигании СНГ
Продукты, образующиеся при сжигании СНГ в газовых приборах, бытовых и промышленных, представляют собой водяной пар, двуокись углерода и тепло, а также обычно очень небольшие количества Монооксид углерода.
При правильной установке и обслуживании работа газового прибора обеспечивает быстрое и эффективное отопление, приготовление пищи, горячую воду и многое другое, а продукты горения не создают опасных ситуаций.
Если прибор неправильно установлен и не обслуживается или был модифицирован, продукты сгорания могут измениться и стать опасными для людей, находящихся рядом с прибором.
Такая простая вещь, как изменение вентиляции (подача свежего воздуха в прибор для поддержания полного сгорания), может привести к неисправности газового прибора и создать опасную ситуацию для окружающих.
Иногда неисправность газового прибора очевидна.
Копоть, красное или желтое пламя или низкая производительность являются индикаторами, но иногда индикаторы отсутствуют.
Если угарный газ (CO) образуется и попадает из прибора в окружающий воздух, это не будет заметно (без запаха и вкуса), но будет очень опасным.
Очень важно, чтобы газовые приборы правильно устанавливались и обслуживались каждые два года, чтобы обеспечить хорошее сгорание и безопасную и эффективную работу.
А как насчет этилмеркаптана?
Этилмеркаптан — отдушка, добавляемая в сжиженный нефтяной газ в целях безопасности.
При сгорании этилмеркаптана на воздухе образуются CO 2 , H 2 0 и SO 2 .
SO 2 является раздражающим соединением, неприятным в большинстве концентраций. Это часть городского смога.
Образование других сульфидов маловероятно.
Незначительные количества этилмеркаптана присутствуют в парах сжиженного нефтяного газа при сгорании.
Таким образом, количество образующихся продуктов ничтожно мало по сравнению с общим количеством продуктов сгорания.
Техническое обслуживание газового оборудования
Надлежащее техническое обслуживание помогает обеспечить правильное сгорание и минимальное образование CO.
Большинство производителей газового оборудования рекомендуют плановое техническое обслуживание каждые 12 или 24 месяца.
Зависит от производителя и модели прибора.
Важно, чтобы ваши газовые приборы обслуживались только квалифицированными специалистами.
В большинстве случаев это лицензированный газовщик или заводской техник.
Основными предупреждающими знаками того, что вашему газовому прибору требуется обслуживание, являются желтое или красное пламя, пламя с желтым горящим кончиком.
Желтая/коричневая сажа, перегорание контрольных ламп, едкий запах и раздражение глаз также являются признаками.
Исключением являются газовые камины и дровяные камины с желтым пламенем.
Вышеуказанные признаки могут свидетельствовать о неполном сгорании.
В результате вы можете тратить газ и/или производить окись углерода.
Последнее представляет собой серьезную проблему безопасности, если это происходит с бытовым прибором.
Если вы наблюдаете любой из этих предупреждающих знаков, вам следует как можно скорее запланировать обслуживание.
Использование одобренных приборов и газовых установщиков
В Австралии действуют одни из самых строгих стандартов в отношении выбросов при сжигании газовых приборов.
Это делает наши внутренние газовые обогреватели очень безопасными в использовании.
Основными газами, вызывающими озабоченность, являются CO (моноксид углерода) и NO X (оксид азота и диоксид азота).
Эти газы могут образовываться при сгорании.
Внутренние газовые обогреватели должны соответствовать или превосходить эти строгие стандарты для сертификации в Австралии.
Покупайте или используйте только проверенные, сертифицированные и маркированные в Австралии газовые приборы.
Другие страны имеют свои собственные системы сертификации.
Убедитесь, что квалифицированный газовый установщик устанавливает ваши газовые приборы и что у вас есть надлежащая вентиляция.
Наконец, при использовании газовых приборов всегда читайте инструкции производителя и следуйте им.
Не используйте наружные газовые обогреватели в помещении
Те же требования не применяются к наружным обогревателям и бытовым приборам.
Предназначены для наружного применения при неограниченной вентиляции. Таким образом, они не обязаны соответствовать стандартам выбросов внутренних обогревателей.
Сюда входят обогреватели, барбекю, печи для пиццы и все другие бытовые приборы.
Если газовый прибор помечен только для использования вне помещений, не используйте его в помещении. Сюда входят полузакрытые помещения без надлежащей вентиляции.
Никогда не используйте открытый газовый прибор в помещении.
Обнаружение угарного газа
Угарный газ не имеет цвета, запаха и вкуса.
Углекислый газ немного менее плотный, чем воздух, поэтому он поднимается вверх.
Он токсичен при концентрации выше примерно 35 частей на миллион.
Смертельно через 30 минут при 4000 частей на миллион. Оно падает до 5 минут при 5000 ppm.
Симптомы отравления угарным газом включают:
- Головные боли
- Тошнота
- Головокружение
- Одышка
- Головокружение и потеря сознания
Немедленно прекратите использование газового прибора при появлении любого из этих симптомов.
Переместитесь в место, где вы можете дышать свежим воздухом и обратиться за медицинской помощью.
Если вы чувствуете запах газа, это не угарный газ, а одорант, добавленный к природному газу или сжиженному нефтяному газу.
Вам следует немедленно разобраться с утечкой газа.
Выключите газ и проветрите комнату, если это безопасно.
Наилучший способ обнаружения угарного газа — детектор СО.
Вы можете купить их в хозяйственных магазинах, а также в интернет-магазинах.
На момент написания этой статьи по крайней мере у одной крупной сети производителей оборудования и у различных интернет-магазинов был выбор моделей по цене менее 50 долларов каждая.
Заключительные мысли
При использовании и обслуживании в соответствии с инструкциями производителя газовые приборы очень безопасны.
Поэтому обязательно соблюдайте график технического обслуживания, рекомендованный производителем прибора.
Также помните, что никогда не пользуйтесь уличными газовыми приборами в помещении.
Ничто не сравнится с теплом газовой плиты, удовольствием от приготовления пищи на газе или прекрасным теплом газового камина. Наслаждаться!
Просмотреть больше блогов о сжиженном нефтяном газе
Комментарии, вопросы или отзывы?
Пожалуйста, напишите нам по адресу: [email protected]
Информация в этой статье получена из различных источников и считается верной на момент публикации. Однако информация может быть не безошибочной и применимой не во всех обстоятельствах.
Однако информация может быть не безошибочной и применимой не во всех обстоятельствах.
Глава 11: Горение (Обновлено 31.05.10)
Глава 11: Горение (Обновлено 31.05.10) Глава 11: Возгорание
(Спасибо
к Дэвид
Bayless за помощь в написании
этот раздел)
Введение – До этого точка теплоты Q во всех задачах и примерах была либо заданной значение или было получено из отношения первого закона. Однако в различных тепловые двигатели, газовые турбины и паровые электростанции полученный в результате процессов сжигания с использованием либо твердого топлива (например, уголь или дрова). жидкое топливо (например, бензин, керосин или дизельное топливо), или газообразное топливо (например, природный газ или пропан).
В этой главе мы познакомимся с химией и
термодинамика горения родовых углеводородных топлив – (C x H y ),
в котором окислителем является кислород, содержащийся в атмосферном воздухе.
Обратите внимание, что мы не будем рассматривать сжигание твердого топлива или
сложные смеси и смеси углеводородов, входящие в состав
бензин, керосин или дизельное топливо.
Атмосферный воздух содержит примерно 21% кислорода (O 2 ) по объему. остальные 79% “других газов” в основном азот (N 2 ), т.е. будем считать, что воздух состоит из 21 % кислорода и 79 % азота. объем. Таким образом, каждый моль кислорода, необходимый для окисления углеводорода, сопровождается 79/21 = 3,76 моль азота. Используя эту комбинацию молекулярная масса воздуха становится 29 [кг/кмоль]. Обратите внимание, что это предполагается, что азот обычно не подвергается никакому химическому воздействию. реакция.
Процесс горения – Основной процесс горения можно описать топливом (т. углеводород) плюс окислитель (воздух или кислород), называемый Реагенты , которые подвергаются химическому процессу с выделением тепла с образованием Продукты сгорания так, чтобы масса сохранялась. в простейший процесс горения, известный как стехиометрический Сгорание , весь углерод в топливе образует двуокись углерода (CO 2 ) и весь водород образует воду (H 2 O) в продуктах, поэтому химическую реакцию можно записать так:
где z известен как стехиометрический коэффициент для окислителя (воздуха)
Обратите внимание, что эта реакция дает пять неизвестных: z, a,
b, c, d, поэтому нам нужно решить пять уравнений. стехиометрический
сжигание предполагает, что в продуктах нет избыточного кислорода, поэтому
d = 0. Остальные четыре уравнения получаем из балансировки числа
атомов каждого элемента в реагентах (углерод, водород, кислород
и азот) с количеством атомов этих элементов в
товары. Это означает, что ни один атом не разрушается и не теряется в
реакция горения.
стехиометрический
сжигание предполагает, что в продуктах нет избыточного кислорода, поэтому
d = 0. Остальные четыре уравнения получаем из балансировки числа
атомов каждого элемента в реагентах (углерод, водород, кислород
и азот) с количеством атомов этих элементов в
товары. Это означает, что ни один атом не разрушается и не теряется в
реакция горения.
Элемент | Сумма в реагентах | = | Сумма в продуктах | Сокращенное уравнение |
Углерод (C) | х |
| а | а = х |
Водород (H) | и |
| 2b | б = у/2 |
Кислород (O) | 2z |
| 2а+б | z = а + b/2 |
Азот (N) | 2(3,76)z |
| 2с | c = 3,76z |
Обратите внимание, что образовавшаяся вода может находиться в виде пара или
жидкой фазы в зависимости от температуры и давления
продукты горения.
В качестве примера рассмотрим стехиометрическое горение метана (СН 4 ) в атмосферном воздухе. Приравнивание моляра коэффициенты реагентов и продуктов получаем:
Теоретическое соотношение воздух-топливо и воздух-топливо -The минимальное количество воздуха, обеспечивающее полное сгорание топлива называется Теоретическая Air (также называемый Стехиометрический воздух ). В этом случае продукты не содержат кислорода. Если мы поставляем меньше, чем теоретический воздух, тогда продукты могут содержать углерод монооксида (CO), поэтому нормальная практика заключается в подаче более теоретический воздух, чтобы предотвратить это явление. это Превышение Air приведет к появлению кислорода в продукты.
Стандартная мера количества воздуха, используемого в процесс сгорания Air-Fuel Соотношение (AF), определяемое следующим образом:
Таким образом, рассматривая только реагенты метана сгорания с теоретическим воздухом, представленным выше, получаем:
Проблема решена 11. 1 – В
этой задачи мы хотим разработать уравнение горения и определить
соотношение воздух-топливо для полного сгорания н-бутана (C 4 Н 10 )
с а) теоретическим воздухом и б) 50% избытком воздуха.
1 – В
этой задачи мы хотим разработать уравнение горения и определить
соотношение воздух-топливо для полного сгорания н-бутана (C 4 Н 10 )
с а) теоретическим воздухом и б) 50% избытком воздуха.
Анализ продуктов сгорания – Горение всегда происходит при повышенных температурах и будем считать, что все продукты сгорания (включая воду пар) ведут себя как идеальные газы. Так как газ у них разный. постоянных, удобно использовать уравнение состояния идеального газа в через универсальную газовую постоянную следующим образом:
При анализе продуктов сгорания имеется интересны несколько пунктов:
1) Что такое объемный процент конкретных продуктов, в частности двуокиси углерода (CO 2 ) и углерод монооксид (СО)?
2) Что такое роса точка водяного пара в продуктах сгорания? Это требует оценка парциального давления паровой составляющей водяного пара продукты.

3) Имеются экспериментальные методы объемного анализ продуктов сгорания, как правило, делается на Сухой Основа , что дает объемный процент всех компонентов, кроме водяного пара. Это позволяет простой метод определения фактического соотношения воздух-топливо и избытка используемого воздуха в процессе горения.
Для идеальных газов мы находим, что мольная доля y i i-го компонента в смеси газов при удельном давлении P
а температура T равна объемной доле этого компонента.
Так как из молярного отношения идеального газа: P.V = N.R у .Т,
у нас есть:
Кроме того, поскольку сумма объемов компонентов V i должны равняться общему объему V, имеем:
Используя аналогичный подход, мы определяем частичную давление компонента с использованием закона парциальных давлений Дальтона:
Проблема решена 11. 2 – В
эта проблема Пропан (C 3 H 8 )
сжигается с 61% избыточного воздуха, который поступает в камеру сгорания при
25°С. Предполагая полное сгорание и полное давление 1 атм.
(101,32 кПа), определите а) соотношение воздух-топливо [кг воздуха/кг топлива], б)
объемный процент двуокиси углерода в продуктах, и c)
температура точки росы продуктов.
2 – В
эта проблема Пропан (C 3 H 8 )
сжигается с 61% избыточного воздуха, который поступает в камеру сгорания при
25°С. Предполагая полное сгорание и полное давление 1 атм.
(101,32 кПа), определите а) соотношение воздух-топливо [кг воздуха/кг топлива], б)
объемный процент двуокиси углерода в продуктах, и c)
температура точки росы продуктов.
Проблема решена 11.3 – В эта проблема Этан (C 2 H 6 ) сжигается атмосферным воздухом, а объемный анализ сухие продукты сгорания дают следующее: 10% CO 2 , 1% CO, 3% O 2 и 86% N 2 . Развивать уравнение горения, и определить а) процент избытка воздух, б) соотношение воздух-топливо, и в) точка росы сгорания товары.
Первый закон анализа горения – Основной целью горения является получение тепла за счет изменения энтальпии от реагентов к продуктам. Из первого закона уравнение в контрольном объеме без учета кинетической и потенциальной энергии изменения и при условии, что работа не выполняется, мы имеем:
, где суммирование проводится по всем продукты (p) и реагенты (r).N относится к количеству молей каждого компонента, а h [кДж/кмоль] относится к молярной энтальпии каждый компонент.
Поскольку существует ряд различных веществ нам необходимо установить общее эталонное состояние для оценки энтальпии, обычно выбирают 25 ° C и 1 атм, что обычно обозначается верхним индексом о. Проф. С. Бхаттачарджи из Государственный университет Сан-Диего разработал экспертную веб-систему в < www.thermofluids.net > называется ТЕСТ ( Т он E Эксперт S система для T (гермодинамика) в который он включил набор таблиц свойств идеального газа, основанных на на энтальпии h или = 0 по этой общей ссылке. Мы адаптировали некоторые из этих таблиц специально для этого раздела, и их можно найти в по следующей ссылке:
Горение Таблицы молярной энтальпии
В качестве примера снова рассмотрим полное сгорание метана (CH 4 ) с теоретическим воздухом:
Обратите внимание, что в реагентах и продуктах
В приведенном выше примере у нас есть основные элементы O 2 и N 2 как
а также соединения CH 4 ,
CO 2 и H 2 O.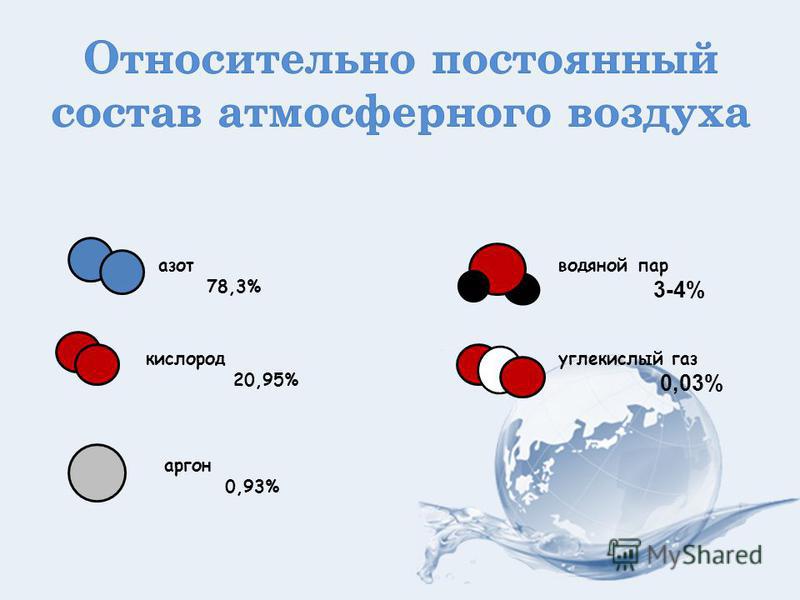 Когда соединение образуется, изменение энтальпии называется Энтальпия
пласта , обозначаемый h f o ,
и для нашего примера:
Когда соединение образуется, изменение энтальпии называется Энтальпия
пласта , обозначаемый h f o ,
и для нашего примера:
Вещество
Формула
hfo [кДж/кмоль]
Углекислый газ
СО 2 (г)
-393 520
Водяной пар
Н 2 О(г)
-241 820
Вода
Н 2 О(л)
-285 820
Метан
CH 4 (г)
-74 850
где (g) относится к газу и (l) относится к жидкость.
Знак минус означает, что процесс Экзотермический , т. е. при образовании соединения выделяется тепло. Обратите внимание, что энтальпия образования основных элементов O 2 и N 2 составляет нуль.
Сначала рассмотрим случай, когда имеется достаточно теплообмен таким образом, что и реагенты, и продукты находятся в 25°C и давление 1 атм, и что водный продукт является жидким. С заметного изменения энтальпии нет, уравнение энергии принимает вид:
Это тепло (Qcv) называется энтальпией . Горения или Нагрева Значение топлива. Если продукты содержат жидкую воду, то это Высшее Теплота сгорания (как в нашем примере), однако, если продукт содержит водяной пар, то это Нижний Теплотворная способность топлива. энтальпия сгорания – это наибольшее количество тепла, которое может быть выделяется данным топливом.
Адиабатическая температура пламени –
Противоположная крайность приведенного выше примера, в котором мы оценивали
энтальпией сгорания является случай адиабатического процесса, в котором
тепло не выделяется. Это приводит к значительной температуре
увеличение продуктов сгорания (обозначается Адиабатическая
Температура пламени ), которая может быть
уменьшается за счет увеличения соотношения воздух-топливо.
Это приводит к значительной температуре
увеличение продуктов сгорания (обозначается Адиабатическая
Температура пламени ), которая может быть
уменьшается за счет увеличения соотношения воздух-топливо.
Решенная проблема 11.4 – Определить адиабатическая температура пламени для полного сгорания Метан ( CH 4 ) с 250% теоретического воздуха в адиабатическом контрольном объеме.
Это уравнение может быть решено только итеративным
метод проб и ошибок с использованием таблиц Sensible
Энтальпия против температуры для всех четырех
составные части продукции – СО 2 ,
Н 2 О, О 2 ,
и N 2 . Быстрый
приближение к адиабатической температуре пламени может быть получено с помощью
при условии, что продукты полностью состоят из воздуха. Этот подход был
представил нас Поттер и Somerton в их Schaum’s
Краткое изложение термодинамики для инженеров ,
в котором они предполагали, что все продукты будут N 2 . Мы находим более удобным использовать воздух, предполагая репрезентативное значение
из конкретных
Теплоемкость воздуха : С р, 1000К = 1,142 [кДж/кг·К].
Мы находим более удобным использовать воздух, предполагая репрезентативное значение
из конкретных
Теплоемкость воздуха : С р, 1000К = 1,142 [кДж/кг·К].
Таким образом, суммируя все моли продуктов, мы имеем:
Использование таблиц Разумный Энтальпия против температуры мы оценили энтальпии всех четырех продуктов при температуре 1280К. Этот в результате общая энтальпия составила 802 410 [кДж/кмоль топлива], что составляет очень близко к требуемому значению, что оправдывает такой подход.
Проблема 11.5 – – Определить адиабатическую температуру пламени. полное сгорание пропана ( C 3 H 8 ) с 250% теоретического воздуха в адиабатическом контрольном объеме [T = 1300К].
__________________________________________________________________________________________
Инженерная термодинамика Израиля
Уриэли находится под лицензией Creative
Commons Attribution-Noncommercial-Share Alike 3. 0 США
Лицензия
0 США
Лицензия
Когда газ пропан C3h8 сжигается с кислородом?
При сгорании газообразного пропана (C3H8) с кислородом образуются двуокись углерода и вода.
Что происходит при взаимодействии C3H8 с кислородом?
Вода и двуокись углерода образуются при взаимодействии газообразного пропана (C 3H 8) с кислородом. При комнатной температуре пропан имеет плотность 2,02 г/л. 3CO 2(г) + 4H 2O из C 3H 8(г) + 5O(г) (ж).
b) Сколько граммов CO 2 образуется из 18,5 г газообразного кислорода и дополнительного количества пропана?
c) Сколько граммов H 2 O может быть получено в результате реакции 8,50 x 10 молекул газообразного пропана?
Сколько молекул углекислого газа образуется при сжигании пропана C3H8?
[Это пригодится в (c) ниже.] Когда один моль пропана C3H8 реагирует с пятью молями кислорода, образуются три моля углекислого газа CO2 и четыре моля воды h3O.
При сжигании сжиженного нефтяного газа образуется угарный газ Выделяется ли сжиженный нефтяной газ угарный газ
Когда приборы, работающие на природном газе или пропане (СНГ), сгорают с неполным сгоранием, образуется угарный газ. Угарный газ если и вырабатывается, то в небольших количествах правильно функционирующими газовыми приборами.
Угарный газ если и вырабатывается, то в небольших количествах правильно функционирующими газовыми приборами.
Неполное и полное сгорание пропана
Процентное содержание СНГ в смеси СНГ с воздухом известно как нижний и верхний пределы воспламеняемости.
Это указывает на то, что LPG должен составлять от 2,15% до 9,6% от общей смеси LPG/воздух, чтобы быть горючим.
Горелка испускает голубое пламя, когда пропан полностью сгорает, выделяя около 25 МДж/л или 49 МДж/кг тепла.
В результате получаются более богатые смеси, ближе к 90,6%, чаще имеют неполное сгорание.
Неполное сгорание характеризуется желтым пламенем, сажей и чрезмерной конденсацией.
Метан имеет идеальную смесь для горения, которая составляет 10,42%.
Полное сгорание пропана EquationCombustion Formula for LPG
При полном сгорании пропана по уравнению пропан сгорает с образованием водяного пара и двуокиси углерода, а также примерно 25 МДж/л или 49 МДж/кг тепла при наличии достаточного количества кислород. И в английском языке, и в химических формулах это полное уравнение горения пропана:
И в английском языке, и в химических формулах это полное уравнение горения пропана:
Уравнение неполного сгорания пропана-сжиженного нефтяного газа
2 C3H8 + 9 O24 CO2 + 2 CO + 8 h3O + Тепло – это уравнение неполного сгорания пропана.
Неполное сгорание происходит, когда для полного сгорания недостаточно кислорода.
Неполное сгорание снова приводит к образованию водяного пара, углекислого газа и тепла.
Продукты сгорания и угарный газ (CO) образуются при сжигании сжиженного нефтяного газа
Когда сжиженный нефтяной газ используется в бытовых и промышленных газовых приборах, он выделяет водяной пар, двуокись углерода и тепло, а также крайне незначительное количество угарного газа.
Работа газового прибора, если он установлен и обслуживается надлежащим образом, обеспечивает быстрое и эффективное отопление, приготовление пищи, горячее водоснабжение и т. д., а результаты горения не создают никаких вредных последствий.
Если прибор неправильно установлен, не обслуживается или модифицируется, продукты горения могут измениться, создавая опасность для тех, кто находится в непосредственной близости от него.
Простое изменение вентиляции (подача свежего воздуха в прибор для обеспечения полного сгорания) может привести к неисправности газового прибора, что представляет опасность для окружающих.
Копоть, красное или желтое пламя или плохая работа — все это симптомы, хотя бывают случаи, когда их не видно.
Если угарный газ (CO) образуется и выходит из устройства в окружающий воздух, это не будет заметно (без запаха или вкуса), но это будет чрезвычайно смертельно.
Газовые приборы необходимо правильно устанавливать и обслуживать каждые два года, чтобы обеспечить правильное горение и безопасную и эффективную работу.
А как насчет этилмеркаптана?
В большинстве концентраций SO2 является раздражающим и неприятным химическим веществом. Это компонент городского смога.
В результате, по сравнению с общими продуктами сгорания, количества образующихся этих соединений ничтожно малы.
Техническое обслуживание газового оборудования
Большинство производителей газового оборудования рекомендуют плановое техническое обслуживание каждые 12–24 месяца.
Очень важно, чтобы обслуживание вашего газового оборудования выполняли только квалифицированные специалисты.
Желтое или красное пламя, а также пламя с желтым горящим кончиком являются ключевыми признаками того, что ваш газовый прибор нуждается в обслуживании.
Желтая/коричневая сажа, перегоревшие контрольные лампы, едкие запахи и раздражение глаз также являются признаками.
Газовые камины и газовые камины с желтым пламенем являются исключением из этого правила.
Использование одобренных приборов и газовых установщиков
Что касается выбросов при сжигании газовых приборов, в Австралии действуют одни из самых строгих правил.
CO (моноксид углерода) и NOX (оксиды азота) являются наиболее опасными газами (оксид азота и диоксид азота).
Для сертификации в Австралии внутренние газовые обогреватели должны соответствовать или превосходить эти строгие требования.
Убедитесь, что ваши газовые приборы установлены лицензированным специалистом по газовым установкам, и что у вас есть соответствующая вентиляция.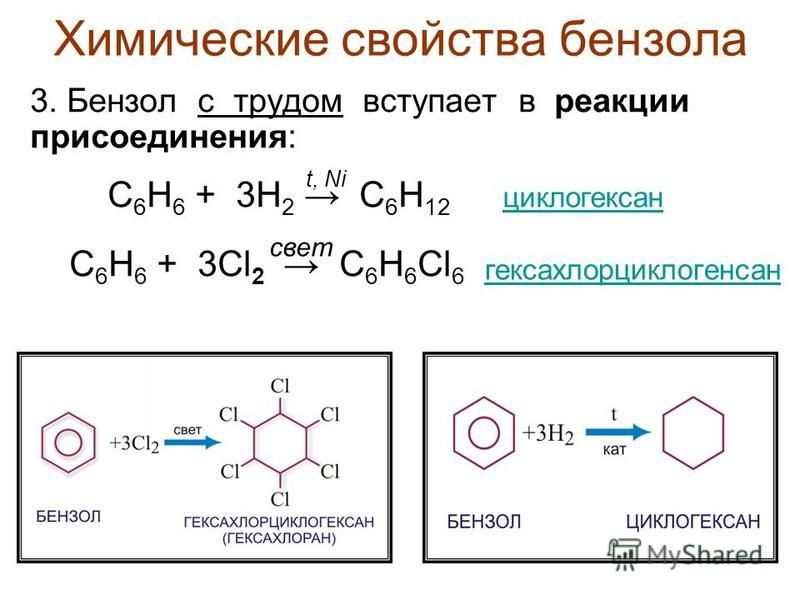
Наконец, всегда читайте и следуйте инструкциям производителя при использовании газового оборудования.
Не используйте наружные газовые обогреватели в помещении
Они предназначены для использования вне помещений и имеют неограниченный поток воздуха. В результате они освобождаются от соблюдения правил выбросов внутренних обогревателей.
Не используйте газовый прибор, на котором указано, что он предназначен для использования вне помещений, исключительно внутри помещений. К ним относятся закрытые помещения с недостаточной вентиляцией.
Обнаружение угарного газа
Отравление угарным газом может вызвать следующие симптомы:
- Проблемы с дыханием
- Потеря сознания и головокружение
Если вы заметили какие-либо из этих симптомов, немедленно выключите газовый прибор.
Вы чувствуете запах газа не угарным газом; это одорант, добавляемый к природному газу или сжиженному нефтяному газу.
На момент написания по крайней мере один крупный розничный продавец аппаратного обеспечения и несколько интернет-магазинов предлагали выбор моделей по цене менее 50 долларов каждая.
Заключительные мысли
Газовые приборы вполне безопасны, если их использовать и обслуживать в соответствии с инструкциями производителя.
Поэтому обязательно соблюдайте рекомендуемый производителем прибора режим обслуживания.
Ничто не сравнится с комфортом газового обогревателя, удовольствием от приготовления пищи на газу или прекрасным теплом газового камина.
Наслаждайтесь!
Какова химическая формула C3H8 O2?
Чтобы сбалансировать эти уравнения, сначала составьте список количества каждого атома в обеих частях уравнения. В этом случае будет так:
Первым шагом будет умножение CO2 на 3, чтобы сбалансировать содержание углерода в продуктах. Новая формула будет
. Теперь, когда углерод сбалансирован, мы можем сосредоточиться на водороде. Мы можем получить 4 молекулы h30, умножив количество воды на стороне продукта на четыре. Это приводит к 8 атомам водорода с обеих сторон уравнения. Затем мы можем проверить наш уровень кислорода.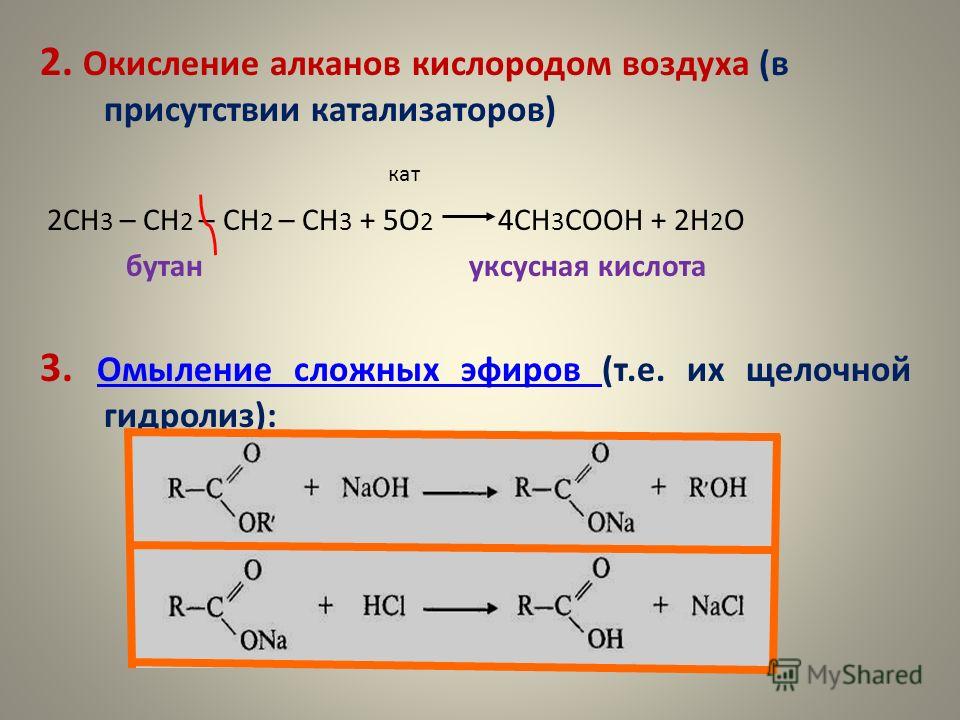 Поскольку на стороне продуктов будет 10 атомов кислорода и 2 на стороне реагентов, мы умножим 02 на стороне реагентов на 5, чтобы уравновесить ситуацию.
Поскольку на стороне продуктов будет 10 атомов кислорода и 2 на стороне реагентов, мы умножим 02 на стороне реагентов на 5, чтобы уравновесить ситуацию.
C3H8 — это тип реакции.
Газообразный пропан (C3H8) образует двуокись углерода и водяной пар при соединении с кислородом воздуха. C3H8(г) + 5O2(г) = 3CO2(г) + 4h3O – сбалансированное уравнение (г) Окислительно-восстановительный потенциал и горение – это два типа классификации.
Образуется ли CO2 при сжигании пропана?
Пропан имеет три атома углерода и восемь атомов водорода в каждой молекуле. По словам Исраэля Уриели из Университета Огайо, топливо в этом примере пропан смешивается с воздухом-окислителем или чистым кислородом во время горения. Поскольку в теоретическом процессе, известном как стехиометрическое сгорание, не остается никакой части исходного топлива, при стехиометрическом сгорании пропана с воздухом образуется не только вода, но и двуокись углерода C2O2, чистый азот N2 и кислород O2. В этом процессе учитываются углерод и водород из пропана, а также азот и дополнительный кислород из воздуха. Пропан легко горит, что делает процесс горения относительно простым в сочетании с воздухом или кислородом. Водный побочный продукт находится в газообразном состоянии при высоких температурах сгорания: водяной пар.
Пропан легко горит, что делает процесс горения относительно простым в сочетании с воздухом или кислородом. Водный побочный продукт находится в газообразном состоянии при высоких температурах сгорания: водяной пар.
полное сгорание пропана (c3h8). сколько граммов воды образуется при
7 680 результатов
Химия
Многие дома в сельской местности Америки отапливаются газом пропаном, соединением, которое содержит только углерод и водород. При полном сгорании образца пропана в качестве единственных продуктов образуется 2,641 грамма двуокиси углерода и 1,422 грамма воды. Найдите эмпирическое
chemisrty
Q5) Реакция сгорания пропана выглядит следующим образом: C3H8 + 5O2 —->>3CO2 + 4h3O 1. Если 20,0 г C3H8 и 20,0 г O2 реагируют, какой реагент является лимитирующим? 2. Сколько граммов воды можно получить? 3. Сколько граммов избытка реактива
Сколько граммов избытка реактива
химия
Многие домашние барбекю работают на пропане (C3H8). Сколько углекислого газа в килограммах образуется при полном сгорании 18,9 л пропана (приблизительное содержание одного 5-галлонного баллона)? Предположим, что плотность жидкого пропана в баллоне
химия
Сколько граммов кислорода требуется для реакции с 2,50 г пропана (C3H8) с образованием УГАРНОГО ГАЗА и воды? это то, что я сделал, почему это неправильно? 2,50 г C3H8 x 1 моль / 44,09г C3H8 x 5 моль O2 / моль = 9,1 г O2 все сокращается, чтобы получить граммы O2, что
химия
Полное сгорание пропана, C3H8(г), представлено уравнением: C3H8(г) + 5 O2(г) → 3 CO2(г) + 4 h3O(ж) ΔH° = -2220 кДж Как сколько теплоты выделяется при полном сгорании 20,0 л C3H8(г) при СТП?
Chem
Кто-нибудь, пожалуйста, объясните мне шаг за шагом, как это сделать. Пропан (C3H8) сгорает в кислороде с образованием углекислого газа и воды. C3H8(г) + 5 O2(г) 3 CO2(г) + 4 h3O(г) Рассчитайте массу CO2, которая может быть получена при реакции 48,2 г пропана
Пропан (C3H8) сгорает в кислороде с образованием углекислого газа и воды. C3H8(г) + 5 O2(г) 3 CO2(г) + 4 h3O(г) Рассчитайте массу CO2, которая может быть получена при реакции 48,2 г пропана
хим
Сжигается 35,00 граммов пропана C3H8. Сколько граммов CO2 ПРОИЗВОДИТСЯ
Химия
Пропан, C3H8, является обычным горючим газом. Используйте следующее, чтобы рассчитать количество граммов пропана, которое вам потребуется для получения 383 кДж тепла. C3H8(г) + 5 O2(г) → 3 CO2(г) + 4 h3O(г) ΔH = −2043 кДж
Химия
Уравнение показывает полное сгорание пропана. C3H8(г) + 5O2(г) –> 3CO2(г) + 4h3O(i) Какое утверждение верно? А) 10 см3 пропана не могут гореть, если присутствует менее 50 см3 кислорода.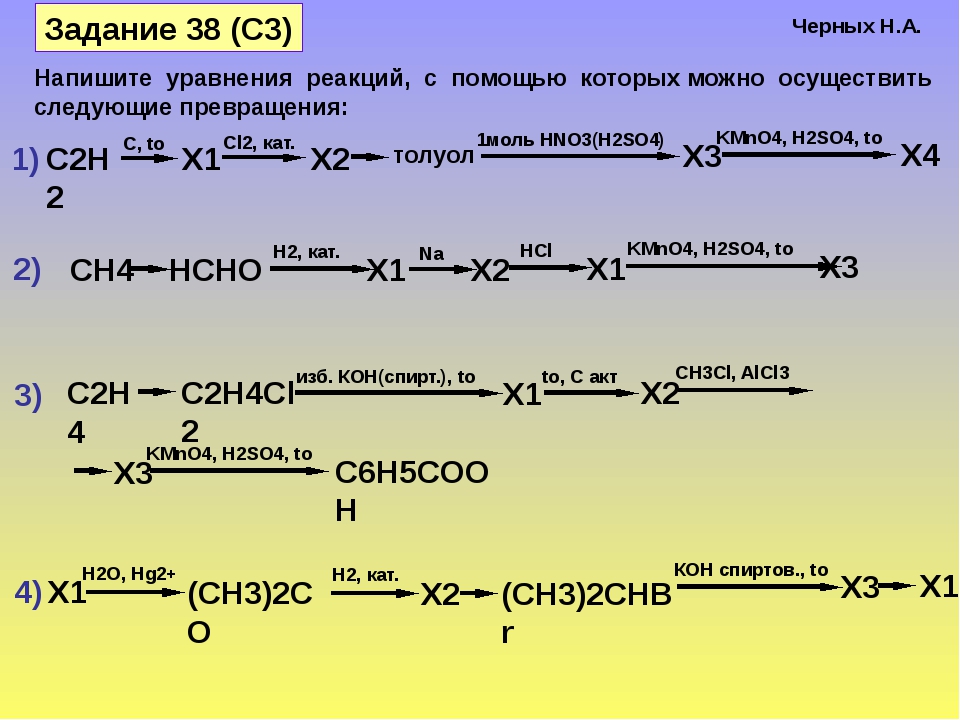 Б) Из 10 см3 пропана получится 40 см3 жидкой воды. В)
Б) Из 10 см3 пропана получится 40 см3 жидкой воды. В)
химия
Если 120 г пропана C3H8 сжечь в избытке кислорода в соответствии со следующим уравнением: C3H8 + 5O2 3CO2 + 4h3O, сколько граммов воды образуется?
Химия
Сколько литров CO2 образуется при полном сгорании C3H8 (пропана) из 10 литров O2?
Chemistry help (DrBob222)
пропан (c3h8) сжигается в кислороде с образованием углекислого газа и воды. Теплота сгорания пропана составляет -2012 кДж/моль. Какое количество теплоты выделится при взаимодействии 3,0 моль C3H8 с 10,0 моль O2? Спасибо, и, пожалуйста, если возможно, показать все шаги!
Химия
Полное сгорание образца пропана дало 2,641 г двуокиси углерода и 1,442 г воды в качестве единственных продуктов. Найдите эмпирическую формулу пропана. Я уже подсчитал количество молей как для воды, так и для углекислого газа. Я также знаю, что
Найдите эмпирическую формулу пропана. Я уже подсчитал количество молей как для воды, так и для углекислого газа. Я также знаю, что
Химия
Рассмотрим сжигание пропана: C3H8(г)+5O2(г) дает 3CO2(г) + 4h3O(л) дельта H= -2221 кДж. Предположим, что все тепло выделяется при сгорании пропана. Рассчитайте дельту H, при которой 5,00 г пропана сгорают в избытке кислорода при постоянном давлении.
химия
рассчитайте минимальное количество граммов пропана, C3H8(g), которое необходимо сжечь, чтобы получить энергию, необходимую для превращения 6,05 кг льда при -24,0 ∘C в жидкую воду при 71,5 ∘C.
хим
при сжигании углеводородов в ограниченном количестве воздуха образуется CO, а также CO2. При сгорании на воздухе 0,450 г определенного углеводорода образовалось 0,467 г СО, 0,733 г СО2 и 0,450 г Н3О. а. Что такое эмпирическая формула? я
При сгорании на воздухе 0,450 г определенного углеводорода образовалось 0,467 г СО, 0,733 г СО2 и 0,450 г Н3О. а. Что такое эмпирическая формула? я
Общая химия
Многие переносные газовые обогреватели и грили используют пропан, C3H8(g). Используя энтальпии образования, рассчитайте количество теплоты, выделяющееся при полном сгорании 16,0 г пропана на воздухе при стандартных условиях. Предположим, что образуется жидкая вода.
Химия
Многие портативные газовые обогреватели и грили используют пропан, C3H8(g). Используя энтальпии образования, рассчитайте количество теплоты, выделяющееся при полном сгорании 19,0 г пропана на воздухе при стандартных условиях. Предположим, что образуется жидкая вода.
Химия
Напишите сбалансированное уравнение сгорания газообразного пропана (C3H8), второстепенного компонента природного газа, в котором он соединяется с газообразным кислородом с образованием газообразного диоксида углерода и газообразной воды. Я ответил C3H8 + 5O2 = 3CO2 + 4h3O но ошибся,
Я ответил C3H8 + 5O2 = 3CO2 + 4h3O но ошибся,
химия
для реакции: c3h8+5o2=3co2 +4h3o сколько молей o2 образуется при полном сгорании 0,75 моль c3h8? Я думаю, что ответ составляет 2,25 моля СО2, но я не уверен, потому что я все еще не думаю, что полностью понимаю это, пожалуйста, помогите
Химия
Помогите, пожалуйста.. 1. Сколько воды можно получить, если начать с 250,0 граммов водорода? 2. Сколько воды вы могли бы получить, если бы начали с 250,0 граммов кислорода? 3. Сколько пропана вам потребуется для производства 1000,0 граммов воды? 4. Сколько из каждого
Химия
При воспламенении смеси 13,0 г ацетилена (C2h3) и 13,0 г кислорода (O2) в результате реакции горения образуются CO2 и h3O.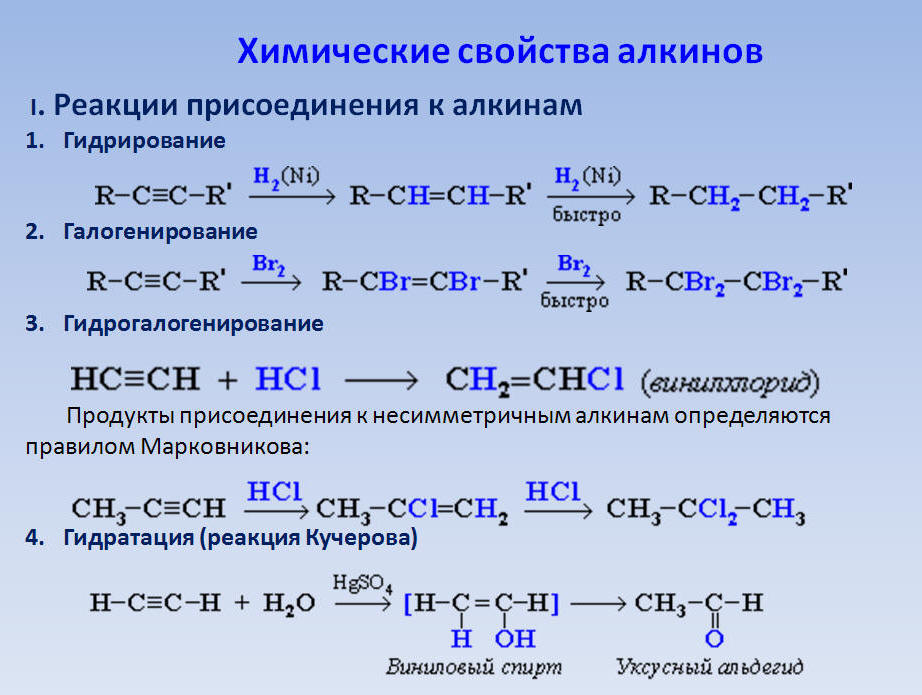 А) Напишите сбалансированное химическое уравнение этой реакции. Б) Какой реагент является лимитирующим? Экспресс в химикате
А) Напишите сбалансированное химическое уравнение этой реакции. Б) Какой реагент является лимитирующим? Экспресс в химикате
химия
Анализ горения, Эмпирические и молекулярные формулы, помогите!? При сжигании 2,686 грамма углеводорода CxHy в приборе для анализа горения образовалось 9,224 грамма CO2 и 1,511 грамма H3O. В отдельном эксперименте молярная масса
химия
От следующего сжигания: 1-бутанол + кислород = двуокись углерода + вода. Сколько граммов углекислого газа и воды образуется при полном сгорании 130,6 граммов 1-бутанола? Помогите мне, пожалуйста! Понятия не имею! Спасибо большое!
Chem
При сгорании пропана (C3H8) образуется CO2 и h3O: C3H8 (г) + 5O2 (г) → 3CO2 (г) + 4h3O (г) В результате реакции 3,5 моль O2 образуется ________ моль h3O.
химия
3. При воспламенении смеси 10,0 г ацетилена (C2h3) и 10,0 г кислорода (O2) в результате реакции горения образуются CO2 и h3O. А) Напишите уравнение этой реакции. Б) Что является лимитирующим реагентом? В) Сколько граммов С2,
Химия
При воспламенении смеси 13,0 г ацетилена (C2h3) и 13,0 г кислорода (O2) в результате реакции горения образуются CO2 и h3O. Сколько граммов C2h3 осталось после завершения реакции? Сколько граммов CO2 присутствует после
химия
если 15 граммов этанового газа c2h6 вступают в реакцию со 128 граммами кислорода в результате реакции горения, сколько молей воды можно получить?
Химия
Пропан и кислород реагируют в соответствии со следующим уравнением. C3H8(г) + 5O2>>>3CO2(г) + 4h3O(г) Рассчитайте объем образовавшихся углекислого газа и водяного пара, а также объем оставшегося кислорода при реакции 20,0 дм3 пропана со 120,0 дм3 кислорода.
C3H8(г) + 5O2>>>3CO2(г) + 4h3O(г) Рассчитайте объем образовавшихся углекислого газа и водяного пара, а также объем оставшегося кислорода при реакции 20,0 дм3 пропана со 120,0 дм3 кислорода.
Помогите пожалуйста!!! Химия
Несколько вариантов При сжигании метана с кислородом образуются углекислый газ и вода. Если из 8 граммов метана и 32 граммов кислорода получить 18 граммов воды, сколько граммов углекислого газа получится в результате реакции? а)40 б)22 в)58
Наука
Рассчитайте количество воды, полученное при сгорании 44 г пропана и 16 г метана.
Подробнее Chem
Рассмотрим горение пропана. Дельта Н составляет -2221 кДж. Предположим, что все тепло выделяется при сгорании пропана. Какую массу пропана необходимо сжечь, чтобы получить это количество энергии, если предположить, что эффективность процесса теплопередачи составляет 60 %.
Какую массу пропана необходимо сжечь, чтобы получить это количество энергии, если предположить, что эффективность процесса теплопередачи составляет 60 %.
химия
при сжигании пропана образуется двуокись углерода и пар C3H8(г)+5O2(г) 3CO2(г)+4h3O(г)
Химия
При соединении 16 граммов метана с 64 граммами кислорода образуется 44 грамма углекислого газа плюс вода. Какая масса воды образуется? Вы можете решить эту задачу как проблему стехиометрии ИЛИ вы можете признать, что закон сохранения массы говорит
химия
какой коэффициент пересчета вы используете в первую очередь для расчета количества граммов CO2, полученного в результате реакции 50,6 граммов Ch5 с O2? Уравнение полного сгорания метана: Ch5+2O2–>CO2+2h3O.
Химия
1. Монооксид азота окисляется на воздухе с образованием коричневого диоксида азота. Начиная с 2,2 моль NO, сколько молей и сколько граммов O2 потребуется для завершения реакции? Какая масса NO2 в граммах образовалась?
химия
Анализ сжигания 1,00 г мужского полового гормона тестостерона дает 2,90 г CO2 и 0,875 г h3O. Каковы массовые проценты углерода, водорода и кислорода в тестостероне? Как мне это решить? Сколько граммов C содержится в 2,90 г CO2? Это
Химия
Используя сбалансированное уравнение реакции для сжигания пропана, определите количество молей кислорода, которое будет реагировать с 0,50 моль пропана, и количество молей углекислого газа, которое будет образовано?
Химия
C3H8 + 5O2 3CO2 + 4h3O Сколько граммов кислорода требуется для сжигания 7,0 г C3H8?
Наука
Во время научной лаборатории, изучающей химические реакции, ученики миссис Грей положили таблетку антацида и пакет Ziploc. Они записали массу таблетки 25 грамм и пакетика 60 грамм. Затем осторожно добавили 50 граммов воды и быстро запечатали
Они записали массу таблетки 25 грамм и пакетика 60 грамм. Затем осторожно добавили 50 граммов воды и быстро запечатали
Наука
Если вода массой 15,0 грамм нагревается до водяного пара в закрытой системе, такой как закрытая стеклянная банка, какова масса газа после того, как вода полностью испарится? A) 13,5 грамм B) 15,0 грамм C) 16,5 грамм D) Масса не может быть определена
ХИМИЯ
CaCO3(s)+2HCl(aq)>CaCl2(aq)+h3O(l)+CO2(g) сколько граммов хлорида кальция будет получено при соединении 30 г карбоната кальция с 13 г соляной кислоты кислота? Какой реагент избыточен и сколько граммов этого реагента останется после
химия
Какая масса в граммах гидроксида натрия (NaOH) образуется при реакции 20 граммов металлического натрия (Na) с избытком воды?
Химия: стоич
4. Предположим, что избыток пропана С3Н8 сгорает в 320 г кислорода. Сколько молей воды при этом образуется? C3H8 + 5 O2 –> 3 CO2 + 4 h3O (1 балл) 6,02 E 23 моль 1600 моль 4,0 моль 8,0 моль
Предположим, что избыток пропана С3Н8 сгорает в 320 г кислорода. Сколько молей воды при этом образуется? C3H8 + 5 O2 –> 3 CO2 + 4 h3O (1 балл) 6,02 E 23 моль 1600 моль 4,0 моль 8,0 моль
химия
Сколько граммов углекислого газа образуется, если 4,4 г пропана реагируют с 16,0 г кислорода с образованием 7,2 г воды?
стехиометрия
Газообразный аммиак реагирует с газообразным кислородом по следующему уравнению: 4Nh4 + 5O2—-4NO + 6h3O а. Сколько молей газообразного кислорода потребуется для реакции с 23 молями аммиака? (29моль) б. Сколько граммов NO образуется при реакции 25 молей газообразного кислорода
Химия
Какой объем газообразного кислорода на СТП потребуется для полного сгорания 39,0 г октана?
химия
Алюминий реагирует с серной кислотой, которая является кислотой в автомобильных аккумуляторах. Если 20,0 граммов Al поместить в раствор, содержащий 115 граммов h3SO4, сколько граммов газообразного водорода получится? Помогите пожалуйста, не знаю как настроить.
Если 20,0 граммов Al поместить в раствор, содержащий 115 граммов h3SO4, сколько граммов газообразного водорода получится? Помогите пожалуйста, не знаю как настроить.
Химия
При сгорании природного газа по уравнению Ch5 + 2 O2 -> CO2 +2·h30 сколько граммов воды образуется при сгорании 0,264 моля Ch5?
Химия
Рассчитайте парциальное давление (в атм) пропана в смеси, содержащей равные массы пропана (C3H8) и бутана (C4h2O) при 18°C и 746 мм рт.ст.
химия
Сколько молей воды образуется при полном сгорании 14,4 г C5h22?
химия
Какая масса воды образуется при полном сгорании 2,50×10-3 метана?
химия
Метанол Ch4Oh может быть получен реакцией монооксида углерода и газообразного водорода в присутствии катализатора. Если 75,00 г монооксида углерода вступают в реакцию со 106,3 г водорода, образуется 68,40 г метанола. Каков процент выхода метанола?
Если 75,00 г монооксида углерода вступают в реакцию со 106,3 г водорода, образуется 68,40 г метанола. Каков процент выхода метанола?
Химия
Многие электростанции производят энергию, сжигая углеродсодержащее топливо, которое также производит CO2. CO2 является парниковым газом, поэтому перепроизводство может иметь негативные последствия для окружающей среды. Используйте данные энтальпии образования для расчета количества молей CO2 (г)
химия
Сколько граммов углекислого газа может образоваться при воспламенении смеси 3,60 г этилена (C2h5) и 2,70 г кислорода при полном сгорании с образованием углекислого газа и воды?
химия
рассмотрим реакцию, в которой 410 граммов Ca(NO3)2 реагируют с нужным количеством металлического лития в одной реакции замещения. 1-сколько граммов лития требуется? 2- сколько граммов каждого продукта можно произвести?
1-сколько граммов лития требуется? 2- сколько граммов каждого продукта можно произвести?
Химия с отличием
Когда горелка Бунзена зажигается, начинается реакция горения газообразного метана в воздухе. Ч5 (г) + 2 О2 (г) СО2 (г) + 2 ч3О (л) Сколько молей воды получится при полном сгорании 4 молей метана? Ответ: 8
химия
Согласно следующей реакции, сколько граммов гидроксида цинка образуется при полной реакции 29,8 граммов воды с избытком оксида цинка? ZnO (т) + h3O (ж) Zn(OH)2 (водн.)
химия
Рассчитайте массу (в граммах) водяного пара, образующегося при сгорании в воздухе 56,0 граммов чистого газообразного водорода. Имея полученную информацию, рассчитайте массу газообразного кислорода, которая потребуется для сжигания 100 граммов газообразного водорода.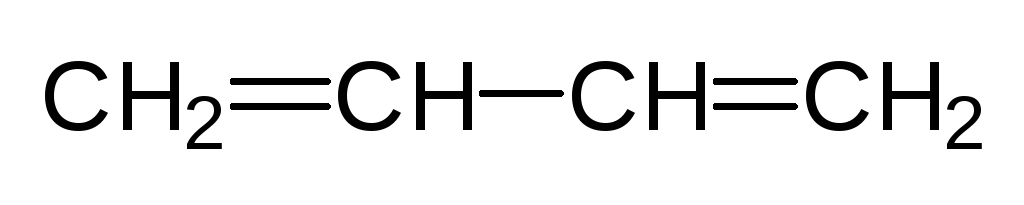
химия
Образец тротила (C7H5N2O6) массой 0,500 г сжигают в бомбовом калориметре, содержащем 610 г воды, при начальной температуре 20,00ºC. Теплоемкость калориметра 420 Дж/°С, теплота сгорания тротила 3374 кДж/моль. Используя эти данные,
Chem
f 147 граммов FeS2 вступают в реакцию с 88 граммами O2 в соответствии со следующим несбалансированным уравнением, сколько граммов Fe2O3 образуется? FeS2 + O2 → Fe2O3 + SO2
Химия
Сколько литров кислорода вступит в реакцию со 124,5 литрами пропана (C3H8) в следующей реакции при нормальных условиях? С3Н8 + 5О2 = 3СО2 + 4ч3О
химия
39,3 грамма c6h6 реагируют со 108,3 граммами o2.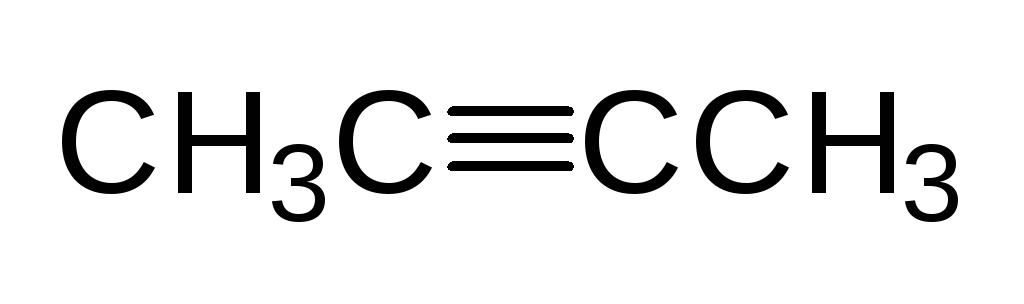 Сколько СО2 образуется в результате этой реакции?
Сколько СО2 образуется в результате этой реакции?
химия
Сколько граммов Nh4 можно получить из 2,89 моль N2 и избытка h3. Выразите ответ численно в граммах.
химия
Сколько граммов Nh4 можно получить из 2,89 моль N2 и избытка h3. Выразите ответ численно в граммах.
chem
Если 34,1 грамма пентана (C5h22) сжечь в избытке кислорода, сколько граммов H3O получится?
Наука
Если 13,8 грамма пентана сжечь в избытке кислорода, сколько граммов воды получится?
Химия
Если 225,0 граммов NO вступают в реакцию с избытком Nh4, сколько граммов H3O образуется
Chem
Сколько молей диоксида серы образуется при получении 72,0 г воды в результате процесса: 2h3S + 3O2 —> 2h3O +2SO2
Химия
Сколько граммов воды получится, если в реакции также образуется 32,0 г закиси азота? используя это уравнение: Nh5NO3 (тв) –> N2O (г) + 2h3O (г)
математика
собака среднего размера весит примерно A.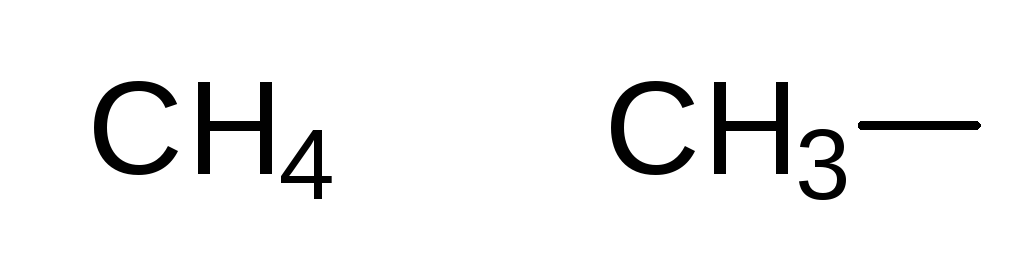 15 грамм B. 50 грамм C. 5000 грамм D. 15,00 грамм Не знаю ответа, помогите
15 грамм B. 50 грамм C. 5000 грамм D. 15,00 грамм Не знаю ответа, помогите
химия
Сколько граммов h3O (Mm = 18,0 г/моль) образуется при сгорании 70,0 г C4h2O (Mm = 58,1 г/моль)? 2C4h20 + 13O2 8CO2 + 10h3O
химия
Гидроксид железа (iii) реагирует с уксусной кислотой с образованием ацетата железа (iii) и воды. Если образуется 45,4 грамма воды, сколько граммов ацетата железа (iii) получится? Fe(OH)3 + 3HC2h3O2 –> Fe(C2h4O2)3 + 3h3O
Химия
Сколько граммов СО2 (Mm = 44,0 г/моль) образуется при сгорании 31,0 г C4h20 (Mm = 58,1 г/моль)?
Химия
Газообразный пропан (C3H8) полностью сгорает в присутствии газообразного кислорода (O2) с образованием газообразного диоксида углерода (CO2) и водяного пара (h3O).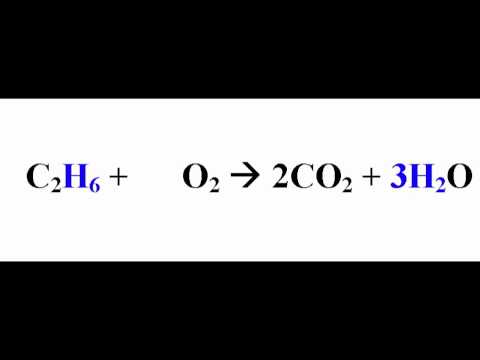 Напишите сбалансированное уравнение этой реакции. Предполагая, что все измерения объема происходят при одной и той же температуре и давлении,
Напишите сбалансированное уравнение этой реакции. Предполагая, что все измерения объема происходят при одной и той же температуре и давлении,
химия
сколько граммов CO2 образуется при взаимодействии 88 граммов O2 с избытком бутана?
Химия
Какой объем кислорода требуется при стандартной температуре и давлении для полного сгорания этанола 2,3 г этанола
химия
Рассчитайте, сколько граммов O2(g) можно получить при нагревании 31,8 граммов KClO3(s).
хим.
Сколько граммов CO2 и граммов H3O образуется при 13,0 г C2h3?
Одаренная и талантливая наука
Какой падающий объект будет иметь наименьшую кинетическую энергию при столкновении с землей? (1 балл) A. 10 граммов воды, падающих со скоростью 1 м/с B. 100 граммов грязи, падающих со скоростью 15 м/с C. 10 граммов грязи, падающих со скоростью 2 м/с*** D. 100 граммов воды , попадая на
10 граммов воды, падающих со скоростью 1 м/с B. 100 граммов грязи, падающих со скоростью 15 м/с C. 10 граммов грязи, падающих со скоростью 2 м/с*** D. 100 граммов воды , попадая на
Math
Мешок муки весит 2,5 кг. Если из 1 мешка получится 5 буханок хлеба, сколько граммов муки потребуется на каждую буханку? A 0,5 грамма B 5 грамм C50 грамм D500 грамм
Химия
Общая реакция элемента, происходящая в щелочной батарее: Zn(s) + MnO2(s) + h3O(l) —> ZnO(s) + Mn(OH)2(s) a) Сколько молей потока электронов на моль реакции?… ответ: 2. Моль е-Примечание: б) Если 6,09г цинка окисляется, сколько граммов марганца
Химия
Если вы начнете с 4,00 моль C3H8 (пропан) и 4,00 моль O2, сколько молей углекислого газа может быть получено?
химия
вода имеет молярную массу 18 грамм это 18 грамм на моль вы выпиваете 2 литровую бутылку воды каждый день и вы такой умный что вы знаете что 1мл воды весит 1 грамм можете вы сказать мне сколько молей воды вы потребляете в день
Химия
Сколько граммов соляной кислоты требуется для полной реакции с 4,30 граммами цинка? Я получил 4,80 г HCl за ответ, но не знаю, как выполнить часть 2, а именно: сколько молекул газа будет произведено? Спасибо.
химия
при сжигании газообразного пропана C3H8 с кислородом образуются углекислый газ и вода. Напишите уравнение несбалансированной формулы реакции.
Химия
Основано на следующем сбалансированном уравнении: 2 Nh4 + 2 O2 –> N2O + 3 h3O a. Сколько молей O2 требуется для полной реакции с 6,00 молями Nh4? б. Сколько граммов O2 требуется для полной реакции с 6,00 моль Nh4? в. Сколько моль H3O
CHEM
1. Сколько теплоты выделяется при реакции 9,22 г глюкозы C6h22O6 по следующему уравнению? C6h22O6 + 6O2 –> 6CO2 + 6h3O ∆H = -2803 кДж 2. Сколько теплоты поглощается при фотосинтезе при образовании 9,22 г глюкозы C6h22O6?
фармацевтические расчеты
1.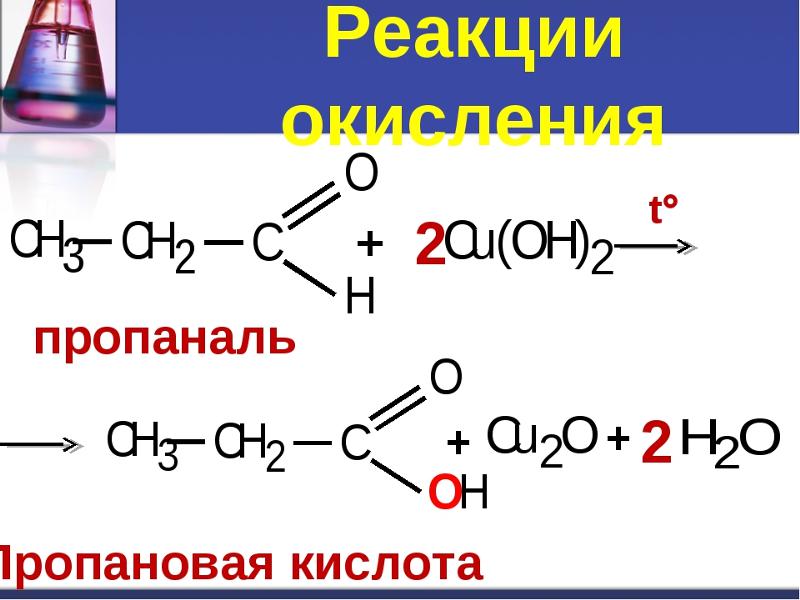 Химический кристалл весит 3,630 г на воздухе и 1,820 г при погружении в масло. Если удельный вес масла равен 0,837, каков удельный вес химического вещества? 2. Кусочек воска в воздухе весит 42,65 грамма, а грузило 38,42 грамма
Химический кристалл весит 3,630 г на воздухе и 1,820 г при погружении в масло. Если удельный вес масла равен 0,837, каков удельный вес химического вещества? 2. Кусочек воска в воздухе весит 42,65 грамма, а грузило 38,42 грамма
Химия
Вот ответы, которые я получил для следующих задач – я прав? 1) Сколько граммов воды, h3O, и пропилена, C3H6, может быть получено при реакции 6,0 г 2-пропанола, C3H8O? C3H8O —-> C3H6 + h3O 1,8 г h3O и 4,2 г C3H6 2) Сколько молей
химия
В эксперименте 3,10 г углерода, водорода и кислорода произвели 4,4 г СО2 и 2,7 г воды при полном сгорании. Определите эмпирическую формулу соединения ( C = 12, 0 = 16, H = 1)
Химия
сколько граммов пропана можно сжечь с 80. 0г кислорода?
0г кислорода?
AP Chemistry
4,50 г фосфата натрия смешивают с 3,75 г нитрата бария. Сколько граммов фосфата бария можно получить?
Математика
Эмпирическое правило: вес в граммах пары почек у взрослых мужчин в возрасте 40 и 49 лет имеет колоколообразное распределение со средним значением 325 граммов и стандартным отклонением 30 граммов. А) Около 95% пар почек будут между
химия
Сколько граммов O2(г) необходимо для полного сгорания 24,0 г C3H8(г)?
химия
. Сколько граммов кислорода требуется для сжигания 47,0 г C3H8?
Химия
Решить Рассчитайте количество граммов углерода в 77,7 г пропана?
химия
4Nh4 + 5O2 = 4NO + 6h3. Газофазная реакция между аммиаком и кислородом протекает только при высокой температуре. Это называется «сжиганием» аммиака, даже если углерод отсутствует. Реакцию проводят в запаянной колбе, изначально содержащей 88,5
Газофазная реакция между аммиаком и кислородом протекает только при высокой температуре. Это называется «сжиганием» аммиака, даже если углерод отсутствует. Реакцию проводят в запаянной колбе, изначально содержащей 88,5
Химия
1. Какова массовая доля раствора, содержащего 50 г растворенного вещества, растворенного в 200 г раствора? Какова концентрация того же раствора в частях на миллион? 2. Какова массовая доля раствора, содержащего 75 г соли
?химия
А) Сколько энергии выделяется при конденсации 25,0 г пара в жидкую воду Н3О при 100°С? Б) Если для повышения температуры воды до 11°С требуется 1215 Дж теплоты, сколько весит вода в граммах? C) Сколько джоулей тепла требуется для получения 1200,00 граммов
Пропан : Ответы по охране труда
Ответы по охране труда Информационные бюллетени
Легко читаемые информационные бюллетени с вопросами и ответами, охватывающие широкий спектр тем по охране труда и технике безопасности на рабочем месте, от опасностей и заболеваний до эргономики и продвижения на рабочем месте. ПОДРОБНЕЕ >
ПОДРОБНЕЕ >
Загрузите бесплатное приложение OSH Answers
Поиск по всем информационным бюллетеням:
Поиск
Введите слово, фразу или задайте вопрос
ПОМОЩЬ
Каковы другие названия или идентифицирующая информация для пропана?
Регистрационный номер CAS : 74-98-6
Другие названия: Диметилметан, н-пропан, пропилгидрид, сжиженный пропан
Основное применение: Топливо, хладагент, аэрозольный пропеллент, растворитель.
Внешний вид: Бесцветный газ.
Запах: Без запаха в естественном состоянии; поэтому имеет ПЛОХИЕ предупреждающие свойства. Отдушка, такая как меркаптан (запах тухлых яиц), используется в большинстве случаев.
ПРИМЕЧАНИЕ. Оборудование, содержащее пропан, может быть загрязнено природным радиоактивным материалом (НОРМ) в виде свинца 210.
Канадский TDG : UN1978
Что такое классификация WHMIS 1988?
А – сжатый газ; B1 — Горючий газ
Класс A
Класс B1
Что нужно знать о пропане в чрезвычайной ситуации?
Аварийный обзор: Бесцветный газ. Без запаха или с добавлением отдушки. ЧРЕЗВЫЧАЙНО ОГНЕОПАСНЫЙ ГАЗ. Возможны дистанционное воспламенение и обратный отсчет. ОПАСНОСТЬ В ЗАМКНУТОМ ПРОСТРАНСТВЕ. Может накапливаться в опасных количествах в низинах, особенно в замкнутых пространствах. СЖАТЫЙ ГАЗ. Содержит газ под давлением. Может взорваться при нагревании. Удушающий. Высокие концентрации могут вытеснять кислород из воздуха и вызывать удушье. Может вызвать обморожение.
Каково потенциальное воздействие пропана на здоровье?
Основные пути воздействия: Вдыхание.
- Вдыхание: Низкие концентрации не опасны.
 Высокая концентрация может вытеснять кислород в воздухе. Если для дыхания доступно меньше кислорода, могут возникнуть такие симптомы, как учащенное дыхание, учащенное сердцебиение, неуклюжесть, эмоциональные расстройства и усталость. Когда кислорода становится меньше, могут возникнуть тошнота и рвота, коллапс, судороги, кома и смерть. Симптомы возникают быстрее при физической нагрузке. Недостаток кислорода может привести к необратимому повреждению органов, включая мозг и сердце. В высоких концентрациях: может нанести вред нервной системе. Симптомы могут включать головную боль, тошноту, головокружение, сонливость и спутанность сознания. Может вызвать нерегулярное сердцебиение.
Высокая концентрация может вытеснять кислород в воздухе. Если для дыхания доступно меньше кислорода, могут возникнуть такие симптомы, как учащенное дыхание, учащенное сердцебиение, неуклюжесть, эмоциональные расстройства и усталость. Когда кислорода становится меньше, могут возникнуть тошнота и рвота, коллапс, судороги, кома и смерть. Симптомы возникают быстрее при физической нагрузке. Недостаток кислорода может привести к необратимому повреждению органов, включая мозг и сердце. В высоких концентрациях: может нанести вред нервной системе. Симптомы могут включать головную боль, тошноту, головокружение, сонливость и спутанность сознания. Может вызвать нерегулярное сердцебиение. - Контакт с кожей: Не раздражает. Прямой контакт со сжиженным газом может вызвать охлаждение или заморозку кожи (обморожение). Симптомы легкого обморожения включают онемение, покалывание и зуд. Симптомы более тяжелого обморожения включают ощущение жжения и скованность. Кожа может стать восково-белой или желтой.
 В тяжелых случаях могут развиваться волдыри, отмирание тканей и инфекция.
В тяжелых случаях могут развиваться волдыри, отмирание тканей и инфекция. - Контакт с глазами: Не раздражает. Прямой контакт со сжиженным газом может заморозить глаза. Это может привести к необратимому повреждению глаз или слепоте.
- Проглатывание: Нерелевантный путь воздействия (газ).
- Последствия длительного (хронического) воздействия: Безвреден.
- Канцерогенность: Не является канцерогеном.
Международное агентство по изучению рака (IARC): Специально не оценивался.
Американская конференция государственных специалистов по промышленной гигиене (ACGIH): специально не назначена.
- Тератогенность/эмбриотоксичность: – Неизвестно, что он причиняет вред нерожденному ребенку.
- Репродуктивная токсичность: Опасность для репродуктивной системы не установлена.
- Мутагенность: Не известно, что это мутаген.

Какие меры первой помощи при пропане?
Вдыхание: Принять меры предосторожности для предотвращения пожара (например, удалить источники возгорания). В случае нехватки кислорода: примите меры предосторожности для обеспечения собственной безопасности перед попыткой спасения (например, наденьте соответствующее защитное снаряжение). Вынести пострадавшего на свежий воздух. Сохраняйте состояние покоя в удобном для дыхания положении. Если дыхание затруднено, обученный персонал должен дать экстренную подачу кислорода. Если сердце остановилось, обученный персонал должен начать сердечно-легочную реанимацию (СЛР) или автоматическую наружную дефибрилляцию (АНД). Немедленно позвоните в токсикологический центр или к врачу. Лечение требуется срочно. Транспортировка в больницу.
Контакт с кожей: Неприменимо (газ). Сжиженный газ: быстро удалить пострадавшего от источника заражения. НЕ пытайтесь согреть пораженный участок на месте. НЕ трите область и не применяйте прямое тепло. Аккуратно снимите одежду или украшения, которые могут ограничивать кровообращение. Аккуратно разрежьте одежду, которая прилипает к коже, и снимите оставшуюся часть одежды. Неплотно накройте пораженный участок стерильной повязкой. НЕ позволяйте пострадавшему пить алкоголь или курить. Немедленно позвоните в токсикологический центр или к врачу. Лечение требуется срочно. Транспортировка в больницу.
НЕ трите область и не применяйте прямое тепло. Аккуратно снимите одежду или украшения, которые могут ограничивать кровообращение. Аккуратно разрежьте одежду, которая прилипает к коже, и снимите оставшуюся часть одежды. Неплотно накройте пораженный участок стерильной повязкой. НЕ позволяйте пострадавшему пить алкоголь или курить. Немедленно позвоните в токсикологический центр или к врачу. Лечение требуется срочно. Транспортировка в больницу.
Контакт с глазами: Неприменимо (газ). Сжиженный газ: вывести пострадавшего на свежий воздух. Немедленно и на короткое время смойте теплой, слегка проточной водой. НЕ пытайтесь согреть. Закройте оба глаза стерильной повязкой. НЕ позволяйте пострадавшему пить алкоголь или курить. Немедленно позвоните в токсикологический центр или к врачу. Лечение требуется срочно. Транспортировка в больницу.
Проглатывание: Неприменимо (газ).
Первая помощь Комментарии: Некоторые из рекомендуемых здесь процедур первой помощи требуют продвинутого обучения оказанию первой помощи. Все процедуры оказания первой помощи должны периодически проверяться врачом, знакомым с химическим веществом и условиями его использования на рабочем месте.
Все процедуры оказания первой помощи должны периодически проверяться врачом, знакомым с химическим веществом и условиями его использования на рабочем месте.
Что такое пожароопасность и средства пожаротушения для пропана?
Воспламеняющиеся свойства: ЧРЕЗВЫЧАЙНО ОГНЕОПАСНЫЙ ГАЗ. Легко может загореться. Легко образует взрывоопасную смесь с воздухом при комнатной температуре.
Подходящие средства пожаротушения: Сухой химический порошок и пена высокой кратности. Следует проконсультироваться с производителями пены для получения рекомендаций относительно типов пены и нормы внесения.
Неподходящие средства пожаротушения: ЗАПРЕЩАЕТСЯ использовать двуокись углерода, пены с низкой кратностью и прямое нанесение воды на сжиженный газ.
Конкретные виды опасности, исходящие от химического вещества: Газ или пар могут перемещаться на значительное расстояние к источнику воспламенения и вспыхивать обратно в место утечки или открытый контейнер. Газ или пар могут скапливаться в опасных количествах в низинах, особенно в замкнутых пространствах, что может представлять опасность для здоровья. Может вытеснять кислород в воздухе, вызывая удушье. Прямое добавление воды к сжиженному газу вызовет мгновенное испарение, приводящее к взрыву (немедленному или отложенному), известному как «взрыв расширяющегося пара кипящей жидкости (BLEVE)». Тепло от огня может вызвать быстрое повышение давления внутри баллонов. Это может привести к взрывному разрыву и внезапному выбросу большого количества газа. Цилиндр может взлететь. При пожаре могут образовываться следующие опасные вещества: очень токсичный угарный газ, двуокись углерода.
Газ или пар могут скапливаться в опасных количествах в низинах, особенно в замкнутых пространствах, что может представлять опасность для здоровья. Может вытеснять кислород в воздухе, вызывая удушье. Прямое добавление воды к сжиженному газу вызовет мгновенное испарение, приводящее к взрыву (немедленному или отложенному), известному как «взрыв расширяющегося пара кипящей жидкости (BLEVE)». Тепло от огня может вызвать быстрое повышение давления внутри баллонов. Это может привести к взрывному разрыву и внезапному выбросу большого количества газа. Цилиндр может взлететь. При пожаре могут образовываться следующие опасные вещества: очень токсичный угарный газ, двуокись углерода.
Каковы опасности стабильности и реакционной способности пропана?
- Химическая стабильность: Обычно стабилен.
- Условия, которых следует избегать: Открытый огонь, искры, статический разряд, тепло и другие источники воспламенения.
- Несовместимые материалы: Повышенный риск возгорания и взрыва при контакте с: окислителями (например, пероксидами), галогенами (например, хлором).
 Не вызывает коррозии: алюминиевых сплавов, углеродистой стали.
Не вызывает коррозии: алюминиевых сплавов, углеродистой стали. - Опасные продукты разложения: Не известны.
- Возможность опасных реакций: Неизвестно.
Каковы меры по предотвращению аварийного выброса пропана?
Индивидуальные меры предосторожности: Немедленно покинуть зону. Изолируйте опасную зону. Не допускайте ненужного и незащищенного персонала. Эвакуируйте места с подветренной стороны. Устраните все источники воспламенения. Используйте заземленное взрывозащищенное оборудование. Возможны дистанционное воспламенение и обратный отсчет. Контролируйте зону на наличие легковоспламеняющейся или взрывоопасной атмосферы. Перед входом, особенно в закрытые помещения, проверьте атмосферу с помощью соответствующего монитора. Тест на достаточный уровень кислорода.
Методы локализации и очистки: Если возможно, поверните протекающий контейнер так, чтобы вышел газ, а не сжиженный газ. Обратитесь в аварийные службы и к производителю/поставщику за консультацией.
Обратитесь в аварийные службы и к производителю/поставщику за консультацией.
Дополнительная информация: Обратитесь за помощью к поставщику, в местные пожарные и аварийно-спасательные службы. При необходимости сообщайте о разливах местным органам здравоохранения, безопасности и охраны окружающей среды.
Какие методы обращения и хранения следует использовать при работе с пропаном?
Обращение: Устраните источники тепла и воспламенения, такие как искры, открытый огонь, горячие поверхности и статический разряд. Разместите таблички «Не курить». Используйте только там, где есть достаточная вентиляция. Немедленно сообщайте об утечках, разливах или отказах предохранительного оборудования (например, системы вентиляции). В случае разлива или утечки немедленно покиньте помещение. Никогда не работайте с системой под давлением. Используйте трубопроводы и оборудование, предназначенные для высоких давлений и низких температур. Изолируйте и продуйте все оборудование, трубопроводы или сосуды перед техническим обслуживанием или ремонтом.
Изолируйте и продуйте все оборудование, трубопроводы или сосуды перед техническим обслуживанием или ремонтом.
ПРИМЕЧАНИЕ. Оборудование, содержащее пропан, может быть загрязнено радиоактивным материалом природного происхождения (НОРМ) в виде свинца 210. Если НОРМ присутствует, при открытии, очистке или ремонте следует принять меры предосторожности для предотвращения вдыхания, контакта с кожей и приема внутрь. работы на внутренних поверхностях этого оборудования.
Хранение: Хранить в прохладном, хорошо проветриваемом месте, вдали от прямых солнечных лучей и источников тепла и воспламенения. Утвержденная, пожаробезопасная зона. Отдельно от несовместимых материалов. (например, кислород, газы хлора) На первом этаже или предпочтительно в изолированном, отдельно стоящем здании. Очистить от горючих и легковоспламеняющихся материалов (например, старых тряпок, картона). Электрически соедините и заземлите контейнеры. Зажимы заземления должны касаться голого металла. Всегда закрепляйте (например, цепью) цилиндры в вертикальном положении на стене, стойке или другой прочной конструкции. Избегайте объемного хранения в помещении.
Всегда закрепляйте (например, цепью) цилиндры в вертикальном положении на стене, стойке или другой прочной конструкции. Избегайте объемного хранения в помещении.
Какой предел воздействия пропана рекомендован Американской конференцией государственных специалистов по промышленной гигиене (ACGIH®)?
ACGIH® TLV® – TWA: Простое удушающее средство*; Опасность взрыва**
Руководство по воздействию Комментарии: Нет конкретного TLV® = пороговое предельное значение. TWA = взвешенное по времени среднее значение.
*Требуется минимальное содержание кислорода.
**Пропан является легковоспламеняющимся удушающим веществом, или выбросы выше ПДК могут приближаться к 10% от нижнего предела взрываемости.
ПРИМЕЧАНИЕ. Во многих (но не во всех) юрисдикциях Канады пределы воздействия аналогичны ACGIH® TLVs®. Поскольку законодательство зависит от юрисдикции, обратитесь в местную юрисдикцию для получения точной информации. Список доступен в Ответах по охране труда о государственных департаментах охраны труда и техники безопасности Канады.
Список актов и правил, регулирующих пределы воздействия химических и биологических агентов, доступен на нашем веб-сайте. Обратите внимание, что, хотя вы можете ознакомиться со списком законодательных актов бесплатно, для просмотра фактической документации вам потребуется подписка.
Какие средства технического контроля для пропана?
Технический контроль: Общей вентиляции обычно достаточно. Не допускайте скопления продукта в воздухе в рабочих или складских помещениях или в замкнутых пространствах. Для крупномасштабного использования этого продукта: используйте строгие меры контроля, такие как ограждение процесса, чтобы предотвратить попадание продукта на рабочее место. Используйте искробезопасные системы вентиляции, утвержденное взрывозащищенное оборудование и искробезопасные электрические системы в местах, где используется и хранится данное изделие. Используйте оборудование для обнаружения утечек и возгорания, а также автоматическую систему пожаротушения. Обеспечьте аварийный душ в рабочей зоне, если существует опасность контакта или разбрызгивания.
Обеспечьте аварийный душ в рабочей зоне, если существует опасность контакта или разбрызгивания.
Какие средства индивидуальной защиты (СИЗ) необходимы при работе с пропаном?
Защита глаз/лица: Не требуется, если продукт используется по назначению.
Защита кожи: Защищайте открытые участки кожи с помощью изолирующих перчаток, подходящих для низких температур, с длинными рукавами, защитным фартуком и брюками, надетыми поверх ботинок или обуви. При работе с баллонами надевайте соответствующую защиту для ног. Подходящие материалы включают: нитриловый каучук, неопреновый каучук. ЗАПРЕЩАЕТСЯ использовать следующие материалы: поливинилхлорид. Рекомендации НЕ действительны для очень тонких перчаток из неопренового каучука и нитрилового каучука (0,3 мм или менее).
Средства защиты органов дыхания:
До 2100 частей на миллион:
(APF = 10) Любой респиратор с подачей воздуха
(APF = 50) Любой автономный дыхательный аппарат с полнолицевой маской
APF = присвоенный коэффициент защиты
3
3 Рекомендации относятся только к респираторам, одобренным Национальным институтом безопасности и гигиены труда (NIOSH).
 Дополнительную информацию см. в Карманном справочнике NIOSH по химическим опасностям.
Дополнительную информацию см. в Карманном справочнике NIOSH по химическим опасностям.Последнее обновление документа: 7 февраля 2020 г.
Добавьте значок на свой веб-сайт или в интранет, чтобы ваши сотрудники могли быстро найти ответы на свои вопросы по охране труда и технике безопасности.
Что нового
Ознакомьтесь с нашим списком «Что нового», чтобы узнать, что было добавлено или изменено.
Нужна дополнительная помощь?
Свяжитесь с нашей информационной линией безопасности
905-572-2981
Бесплатный номер 1-800-668-4284
(в Канаде и США)
Расскажите нам, что вы думаете
Как мы можем сделать наши услуги более полезными для вас? Свяжитесь с нами, чтобы сообщить нам.
Сопутствующие товары и услуги
Вас также могут заинтересовать следующие сопутствующие товары и услуги CCOHS:
Отказ от ответственности
Несмотря на то, что предпринимаются все усилия для обеспечения точности, актуальности и полноты информации, CCOHS не гарантирует, не гарантирует, не заявляет и не ручается за правильность, точность или актуальность предоставленной информации.


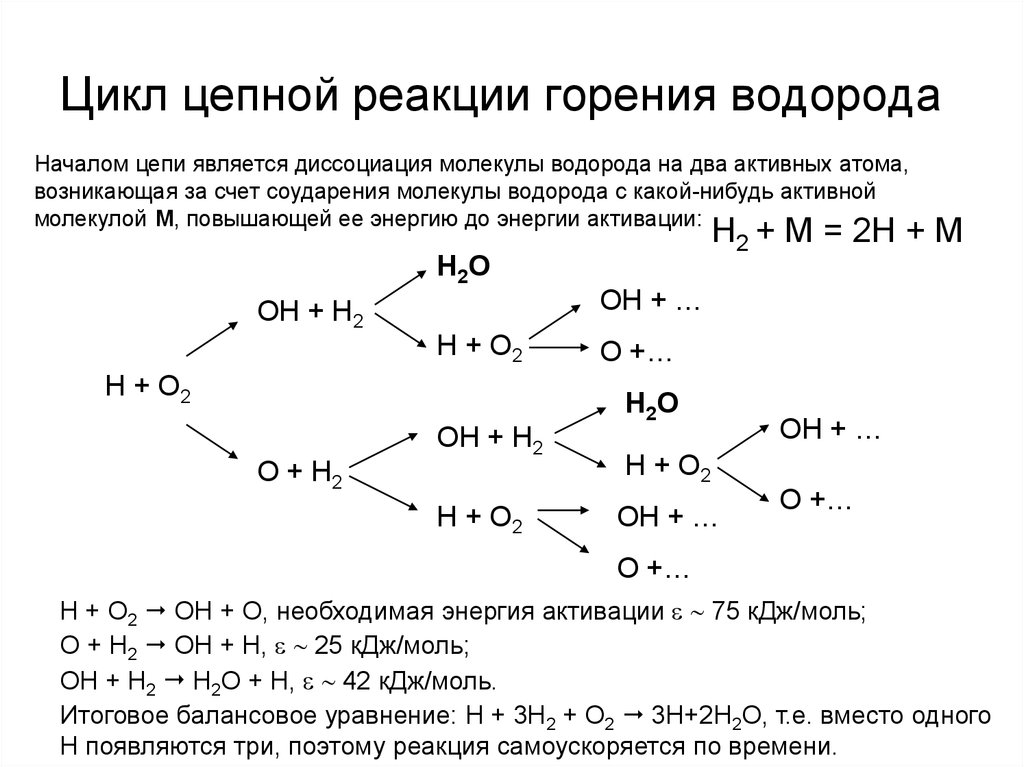

 N относится к количеству молей
каждого компонента, а h [кДж/кмоль] относится к молярной энтальпии
каждый компонент.
N относится к количеству молей
каждого компонента, а h [кДж/кмоль] относится к молярной энтальпии
каждый компонент.